
分析 向盛有20mL 0.1mo1•L-1的稀硫酸的两个烧杯中分别逐滴加入(1)0.1mol•L-1的Ba(0H)2溶液20mL,则硫酸和氢氧化钡之间反应生成硫酸钡和水,硫酸钡是难溶物,水是极弱的电解质;(2)0.1mol•L-1的Bacl2溶液20mL,则硫酸和氯化钡之间反应生成硫酸钡和盐酸,盐酸是强电解质.
解答 解:向盛有20mL 0.1mo1•L-1的稀硫酸的两个烧杯中分别逐滴加入:
(1)0.1mol•L-1的Ba(0H)2溶液20mL,则硫酸和氢氧化钡之间反应生成硫酸钡和水,硫酸钡是难溶物,水是极弱的电解质,所以溶液中自由移动离子浓度减小,导电能力逐渐减弱至零;
(2)0.1mol•L-1的Bacl2溶液20mL,则硫酸和氯化钡之间反应生成硫酸钡和盐酸,盐酸是强电解质,物质的量浓度和氯化钡的相等,所以溶液中自由移动离子浓度减小,导电能力逐渐减弱;
答:两个烧杯中反应后的溶液中自由移动离子浓度均减小,导电能力减弱.
点评 本题考查学生溶液的导电能力和自由移动离子浓度之间的关系知识,注意知识的迁移应用是关键,难度中等.


科目:高中化学 来源: 题型:多选题
| A. | 青铜、不锈钢和硬铝都是合金 | |
| B. | 铝可用于制造燃烧弹和信号弹 | |
| C. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用,因此铝罐可久盛食醋 | |
| D. | 铜锈的主要成分是Cu2(OH)2CO3,可以用稀盐酸除铜锈 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4和C4H8 | B. | CH4和C3H6 | C. | C2H6和C3H6 | D. | C2H6和C4H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
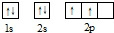
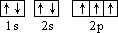 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知六方氮化硼类似于石墨的结构,如图所示,利用所学知识结合该图回答下列问题.
已知六方氮化硼类似于石墨的结构,如图所示,利用所学知识结合该图回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeBr2溶液中通入过里Cl2:2Fe++2Br-+2Cl2=2Fe+Br2+4Cl- | |
| B. | 向FeCl3溶液中加入Mg(OH)2:3 Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ | |
| C. | NaHSO4溶液中滴加Ba(OH)2溶液至中性:H++OH-+SO42-+Ba2+=BaSO4↓+H2O | |
| D. | NaHCO3溶液与NaAlO2溶液反应:HCO3-+AlO2-+H2O=Al(OH)3↓+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com