
| A. | X与Y形成化合物时X显负价,Y显正价 | |
| B. | 第一电离能X大于Y | |
| C. | 最高价氧化物对应的水化物的酸性:X强于Y | |
| D. | 气态氢化物的稳定性:HmX强于HmY |
分析 X、Y元素同周期,且电负性X>Y,则非金属性X>Y.
A.电负性大的元素在化合物中显负价;
B.一般非金属性强的,其第一电离能大,但是第IIA和IIIA,第VA和VIA反常;
C.非金属性越强,最高价氧化物对应的水化物的酸性越强;
D.非金属性越强,气态氢化物越稳定.
解答 解:X、Y元素同周期,且电负性X>Y,则非金属性X>Y.
A.电负性大的元素在化合物中显负价,所以X和Y形成化合物时,X显负价,Y显正价,故A正确;
B.一般非金属性强的第一电离能大,但特殊O的非金属性比N大,但第一电离能N>O,所以第一电离能可能Y小于X,故B错误;
C.非金属性越强,最高价氧化物对应的水化物的酸性,则最高价氧化物对应的水化物的酸性:X强于Y,故C正确;
D.非金属性越强,气态氢化物越稳定,则气态氢化物的稳定性:HmY小于HnX,故D正确;
故选B.
点评 本题考查位置、结构、性质,明确同周期位置关系及电负性大小得出元素的非金属性是解答本题的关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 氧化性(酸性溶液):FeCl3>Co(OH)3>I2 | B. | 还原性(碱性溶液):Fe(OH)2>I2>KIO3 | ||
| C. | 热稳定性:NaCl>NaClO>NaClO4 | D. | 酸性(水溶液):H2CO3>HSCN>HCN |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
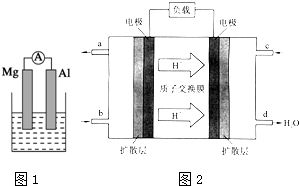 据图回答下列问题:
据图回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应结束后溶液的pH:甲>乙 | |
| B. | 反应开始时的速率:甲>乙 | |
| C. | 反应所需时间:甲<乙 | |
| D. | 反应开始时,酸的物质的量浓度:甲>乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤代烃都可发生取代反应 | |
| B. | 由2-氯丙烷制取少量的1,2-丙二醇时,只需要经过取代反应、水解反应 | |
| C. | 实验室制硝基苯时,正确的操作顺序应该是先加入苯,再滴加浓硫酸,最后滴加浓硝酸 | |
| D. | 2-甲基-2-丁烯可以形成顺反异构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4HCO3和盐酸的反应是放热反应 | |
| B. | 该反应中,热能转化为产物内部的能量 | |
| C. | 反应物的总能量高于生成物的总能量 | |
| D. | 该反应可以设计成原电池来提供电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 4.6 g NO2与N2O4的混合物中含有的N原子数为0.1NA | |
| B. | 常温常压下,22.4 L NO的分子数为0.1NA | |
| C. | 将0.3mol NO2溶于水,完全反应后,转移的电子数为0.2 NA | |
| D. | 1L0.1mol•L-1 氨水中含有的NH3分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业生产玻璃、水泥、漂白粉,均需要用石灰石为原料 | |
| B. | CO会与血红蛋白结合,使人中毒;可将中毒病人放入氧仓中解毒,其解毒原理符合平衡移动原理 | |
| C. | 2011年5月份起,面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,CaO2属于碱性氧化物 | |
| D. | 固体煤经处理变为气体燃料后,可以减少SO2和烟尘的排放,且燃烧效率提高,有利于“节能减排” |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com