
”¾ĢāÄæ”æŅŌĻĀŹōÓŚ¹²¼Ū»ÆŗĻĪļµÄŹĒ£Ø £©
A.NH4ClB.½šøÕŹÆC.Al2O3D.HCl
 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ŌÓŚ²»Ķ¬ŌŖĖŲµÄŌ×Ó£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A.ÖŹ×ÓŹżŅ»¶Ø²»µČB.ÖŠ×ÓŹżŅ»¶Ø²»µČ
C.ŗĖĶāµē×ÓŹżŅ»¶ØĻąµČD.ÖŹĮæŹżŅ»¶Ø²»µČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĢå»żæɱäµÄĆܱÕČŻĘ÷Ź¢ÓŠŹŹĮæµÄAŗĶBµÄ»ģŗĻĘųĢ壬ŌŚŅ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦£ŗA(g)+3B(g)![]() 2C(g)£¬ČōĪ¬³ÖĪĀ¶ČŗĶŃ¹Ēæ²»±ä£¬µ±“ļµ½Ę½ŗāŹ±£¬ČŻĘ÷µÄĢå»żĪŖ2L£¬ĘäÖŠCĘųĢåµÄĢå»żÕ¼10%£¬ĻĀĮŠĶʶĻÕżČ·µÄŹĒ
2C(g)£¬ČōĪ¬³ÖĪĀ¶ČŗĶŃ¹Ēæ²»±ä£¬µ±“ļµ½Ę½ŗāŹ±£¬ČŻĘ÷µÄĢå»żĪŖ2L£¬ĘäÖŠCĘųĢåµÄĢå»żÕ¼10%£¬ĻĀĮŠĶʶĻÕżČ·µÄŹĒ
¢ŁŌ»ģŗĻĘųĢåµÄĢå»żĪŖ2.4L ¢ŚŌ»ģŗĻĘųĢåµÄĢå»żĪŖ2.2L
¢Ū·“Ó¦“ļĘ½ŗāŹ±£¬ĘųĢåAĻūŗĵō0.1L ¢Ü·“Ó¦“ļĘ½ŗāŹ±£¬ĘųĢåBĻūŗĵō0.1L
A. ¢Ś¢Ū B. ¢Ś¢Ü C. ¢Ł¢Ū D. ¢Ł¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢå»ż²»±äµÄĆܱÕČŻĘ÷ÖŠ³äČėH2ŗĶI2 £¬ ·¢Éś·“Ó¦H2£Øg£©+I2£Øg£© 2HI£Øg£©£»£ØÕż·“Ó¦ĪŖĪüČČ·“Ó¦£©£¬µ±“ļµ½Ę½ŗāŗó£¬t0Ź±ÉżøßĪĀ¶Č£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.ČŻĘ÷ÄŚĘųĢåŃÕÉ«±äÉī£¬Ę½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»±ä
B.Ę½ŗā²»ŅĘ¶Æ£¬»ģŗĻĘųĢåĆܶČŌö“ó
C.H2×Ŗ»ÆĀŹŌö“ó£¬HIĘ½ŗāÅØ¶Č±äŠ”
D.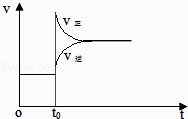 øıäĢõ¼žĒ°ŗó£¬ĖŁĀŹĶ¼ĻńĪŖ£ØČēĶ¼£©
øıäĢõ¼žĒ°ŗó£¬ĖŁĀŹĶ¼ĻńĪŖ£ØČēĶ¼£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃé²Ł×÷ÖŠÕżČ·µÄŹĒ£Ø””””£©
A. Õō·¢²Ł×÷Ź±£¬Ó¦Ź¹»ģŗĻĪļÖŠµÄĖ®·ÖĶźČ«ÕōøÉŗ󣬲ÅÄÜĶ£Ö¹¼ÓČČ
B. ÕōĮ󏱥äĖ®“ÓĄäÄż¹ÜĻĀæŚČė£¬ÉĻæŚ³ö
C. ·ÖŅŗ²Ł×÷Ź±£¬·ÖŅŗĀ©¶·ÖŠĻĀ²ćŅŗĢå“ÓĻĀæŚ·Å³ö£¬Č»ŗó»»Ņ»øö½ÓŹÕĘ÷£¬ŌŁ·Å³öÉĻ²ćŅŗĢå
D. ŻĶČ”²Ł×÷Ź±£¬Ó¦Ń”ŌńÓŠ»śŻĶČ”¼Į£¬ĒŅŻĶČ”¼ĮµÄĆܶȱŲŠė±ČĖ®“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČĖĆĒ³£ÓĆ“ß»Æ¼ĮĄ“Ń”Ōń·“Ó¦½ųŠŠµÄ·½Ļņ£®ČēĶ¼ĖłŹ¾ĪŖŅ»¶ØĢõ¼žĻĀ1mol CH3OHÓėO2·¢Éś·“Ó¦Ź±£¬Éś³ÉCO”¢CO2»ņHCHOµÄÄÜĮæ±ä»ÆĶ¼[·“Ó¦ĪļO2£Øg£©ŗĶÉś³ÉĪļH2O£Øg£©ĀŌČ„]£®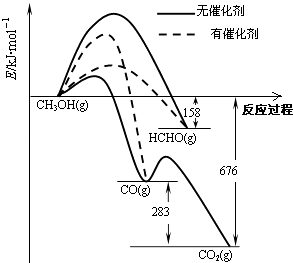
£Ø1£©¢ŁŌŚÓŠ“߻ƼĮ×÷ÓĆĻĀ£¬CH3OHÓėO2·“Ó¦Ö÷ŅŖÉś³É£ØĢī”°CO”¢CO2”±»ņ”°HCHO”±£©£®2HCHO£Øg£©+O2£Øg£©ØT2CO£Øg£©+2H2O£Øg£©”÷H= £®
¢Ś¼×“¼ÖĘČ”¼×Č©æÉÓĆAg×÷“߻ƼĮ£¬ŗ¬ÓŠAgCl»įÓ°ĻģAg“߻ƼĮµÄ»īŠŌ£®ÓĆ°±Ė®æÉŅŌČܽā³żČ„ĘäÖŠµÄAgCl£¬Š“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ £®
£Ø2£©ŅŃÖŖ£ŗCO£Øg£©+2H2£Øg£©CH3OH£Øg£©”÷H=©a kJmol©1 £®
¢Ł¾²ā¶Ø²»Ķ¬ĪĀ¶ČĻĀøĆ·“Ó¦µÄĘ½ŗā³£ŹżČēĻĀ£ŗ
ĪĀ¶Č£Ø”ę£© | 250 | 300 | 350 |
K | 2.041 | 0.270 | 0.012 |
ČōijŹ±æĢ”¢250”ę²āµĆøĆ·“Ó¦µÄ·“Ó¦ĪļÓėÉś³ÉĪļµÄÅضČĪŖc£ØCO£©=0.4molL©1”¢c£ØH2£©=0.4molL©1”¢c£ØCH3OH£©=0.8molL©1 £¬ Ōņ“ĖŹ±vÕżvÄę£ØĢī”°£¾”±”¢”°£¼”±»ņ”°=”±£©£®
¢ŚÄ³ĪĀ¶ČĻĀ£¬ŌŚĢå»ż¹Ģ¶ØµÄ2LµÄĆܱÕČŻĘ÷ÖŠ½«1mol COŗĶ2mol H2»ģŗĻ£¬²āµĆ²»Ķ¬Ź±æĢµÄ·“Ó¦Ē°ŗóŃ¹Ēæ¹ŲĻµČēĻĀ£ŗ
Ź±¼ä£Ømin£© | 5 | 10 | 15 | 20 | 25 | 30 |
Ń¹Ēæ±Č£ØPŗó/PĒ°£© | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
Ōņ0”«15min£¬ÓĆH2±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ £¬ “ļµ½Ę½ŗāŹ±COµÄ×Ŗ»ÆĀŹĪŖ £®
£Ø3£©ĄūÓĆÄĘ¼īŃ»··ØæɳżČ„SO2 £¬ Ļū³żSO2¶Ō»·¾³µÄĪŪČ¾£®ĪüŹÕŅŗĪüŹÕSO2µÄ¹ż³ĢÖŠ£¬pHĖęn£ØSO32©£©£ŗn£ØHSO3©£©±ä»Æ¹ŲĻµČēĻĀ±ķ£ŗ
n£ØSO32©£©£ŗn£ØHSO3©£© | 91£ŗ9 | 1£ŗ1 | 1£ŗ91 |
pH | 8.2 | 7.2 | 6.2 |
¢Łøł¾ŻÉĻ±ķÅŠ¶ĻNaHSO3ČÜŅŗĻŌŠŌ£®
¢ŚŌŚNaHSO3ČÜŅŗÖŠĄė×ÓÅØ¶Č¹ŲĻµÕżČ·µÄŹĒ £ØĢī×ÖÄø£©£®
a£®c£ØNa+£©=2c£ØSO32©£©+c£ØHSO3©£©
b£®c£ØNa+£©£¾c£ØHSO3©£©£¾c£ØH+£©£¾c£ØSO32©£©£¾c£ØOH©£©
c£®c£ØH2SO3£©+c£ØH+£©=c£ØSO32©£©+£ØOH©£©
d£®c£ØNa+£©+c£ØH+£©=c£ØSO32©£©+c£ØHSO3©£©+c£ØOH©£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³ŃŠ¾æŠŌѧĻ°Š”×éÉč¼ĘĮĖŅ»×鏵ŃéŃéÖ¤ŌŖĖŲÖÜĘŚĀÉ”£
(1)¼×Ķ¬Ń§ŌŚa”¢b”¢c”¢dĖÄÖ»ÉÕ±ÖŠ·Ö±š¼ÓČė50mLĄäĖ®£¬ŌŁ·Ö±šµĪ¼Ó¼øµĪ·ÓĢŖŹŌŅŗ£¬ŅĄ“Ī¼ÓČė“óŠ”Ļą½üµÄÄĘ(Na)”¢Ć¾(Mg)”¢ĀĮ(Al)”¢¼Ų(K)½šŹōŠ”æ飬¹Ū²ģĻÖĻó”£
¢Ł¼×Ķ¬Ń§Éč¼ĘŹµŃéµÄÄæµÄŹĒ£ŗŃŠ¾æĶ¬Ņ»ÖÜĘŚ¼°Ķ¬Ņ»Ö÷×壬½šŹōŌŖĖŲµÄŌ×Ó_______ µē×ÓÄÜĮ¦µŻ±ä¹ęĀÉ”£
¢ŚŹµŃéÖŠ·¢ĻÖb”¢cĮ½Ö»ÉÕ±ÖŠ¼øŗõƻӊŹ²Ć“ĻÖĻó£¬ŅŖĻė“ļµ½ŹµŃéÄæµÄ£¬ĒėÄć°ļ֜єŌńĻĀĮŠŗĻŹŹµÄ·½·Ø__(Ģī×ÖÄøŠņŗÅ)”£
A.°ŃĆ¾”¢ĀĮµÄ½šŹōæé»»³É½šŹō·ŪÄ©
B.°ŃÉÕ±ÖŠµÄĄäĖ®»»³ÉČČĖ®
C.°ŃÉÕ±ÖŠµÄĄäĖ®»»³ÉŃĪĖį
D.°ŃÉÕ±ÖŠµÄĄäĖ®»»³ÉĒāŃõ»ÆÄĘČÜŅŗ
¢ŪŠ“³ödÉÕ±ÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½____________________”£
(2)ŅŃÖŖŌŖĖŲ·Ē½šŹōŠŌŌ½Ē棬Ęä×īøß¼Ūŗ¬ŃõĖįµÄĖįŠŌ¾ĶŌ½Ē攣ŅŅĶ¬Ń§Éč¼ĘĮĖĻĀĶ¼×°ÖĆŅŌŃéÖ¤Ģ¼”¢µŖ”¢¹čŌŖĖŲµÄŌ×ӵķĒ½šŹōŠŌĒæČõ”£
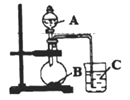
ŅŅĶ¬Ń§Éč¼ĘµÄŹµŃéæÉÖ±½ÓÖ¤Ć÷ČżÖÖĖįµÄĖįŠŌĒæČõ£¬ŅŃÖŖAŹĒŅ»ÖÖĒæĖį£¬³£ĪĀĻĀæÉÓėĶ·“Ó¦£»BŹĒæéד¹ĢĢ壻ÉÕ±ÖŠŹ¢·ÅCµÄČÜŅŗ”£“ņæŖ·ÖŅŗĀ©¶·µÄ»īČūŗó£¬æɹŪ²ģµ½ÉÕ±ÖŠÓŠ°×É«³ĮµķÉś³É”£
¢ŁŠ“³öĖłŃ”ÓĆĪļÖŹµÄ»ÆѧŹ½£ŗA__________”¢C_________________£»
¢ŚŠ“³öÉÕ±ÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ____________________”£
(3)±ūĶ¬Ń§ČĻĪŖŅŅĶ¬Ń§µÄŹµŃé·½°ø²»ÄÜ“ļµ½ŹµŃéÄæµÄ£¬»¹Šč²ÉČ”µÄøĽų“ėŹ©ĪŖ£ŗ_______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£Ø £©
A. ±ź×¼×“æöĻĀ£¬1LHClŗĶ1LH2OµÄĪļÖŹµÄĮæĻąĶ¬
B. ±ź×¼×“æöĻĀ£¬1gH2ŗĶ14gN2µÄĢå»żĻąĶ¬
C. 28gCOµÄĢå»żĪŖ22.4L
D. Į½ÖÖĪļÖŹµÄĪļÖŹµÄĮæĻąĶ¬£¬ŌņĖüĆĒŌŚ±ź×¼×“æöĻĀµÄĢå»żŅ²ĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com