
【题目】有机物的种类繁多,包含烃和烃的衍生物,官能团决定有机物的化学性质,请按要求回答下列问题。
I.已知乙二醇( ![]() )、丙三醇(
)、丙三醇(![]() )都与乙醇含有相同的官能团,都属于醇类物质,与乙醇具有相似的化学性质。
)都与乙醇含有相同的官能团,都属于醇类物质,与乙醇具有相似的化学性质。
请按要求完成下列问题:
(1)写出醇类物质都含有的官能团的电子式_______________。
(2)乙醇、乙二醇( ![]() )、丙三醇(
)、丙三醇(![]() )别与足量金属钠作用,产生等量的氢气。则这三种醇的物质的量之比为______。
)别与足量金属钠作用,产生等量的氢气。则这三种醇的物质的量之比为______。
(3)写出乙醇的催化氧化的化学方程式__________,反应类型:________ ;
(4)丙三醇(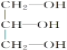 )与足量乙酸发生酯化反应的化学方程式(反应条件与乙醇酯化反应相同)_____。
)与足量乙酸发生酯化反应的化学方程式(反应条件与乙醇酯化反应相同)_____。
II.以下是用苯作原料制备一系列化合物的转化关系图,已知:R-NO2![]() R-NH2(其中-R代表烃基)
R-NH2(其中-R代表烃基)
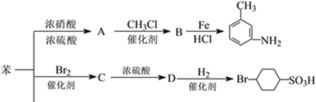
(5)写出A→B的化学反应方程式______,反应类型:_________。
(6)C中含有的官能团的名称为________;D的结构简式为______。
【答案】![]() 6:3:2 2CH3CH2OH+O2
6:3:2 2CH3CH2OH+O2![]() 2CH3CHO+2H2O 氧化反应
2CH3CHO+2H2O 氧化反应 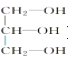 +3CH3COOH
+3CH3COOH![]()
 +3H2O
+3H2O ![]() +CH3Cl
+CH3Cl ![]()
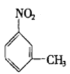 +HCl 取代反应 溴原子
+HCl 取代反应 溴原子 ![]()
【解析】
I.根据官能团(羟基)的结构及醇类性质分析解答;
II.根据转化关系图分析,苯在浓硫酸和浓硝酸的作用下发生取代反应生成A(硝基苯),根据产物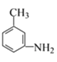 的结构分析,硝基苯与CH3Cl发生间位取代反应生成
的结构分析,硝基苯与CH3Cl发生间位取代反应生成 ,根据题给反应信息知,
,根据题给反应信息知, 被还原生成
被还原生成 ;苯液溴在催化剂条件下发生取代反应生成C(溴苯),溴苯在浓硫酸作用下发生磺化反应生成D(4-溴苯磺酸),D中苯环与氢气发生加成反应,最终生成
;苯液溴在催化剂条件下发生取代反应生成C(溴苯),溴苯在浓硫酸作用下发生磺化反应生成D(4-溴苯磺酸),D中苯环与氢气发生加成反应,最终生成![]() ,据此分析解答。
,据此分析解答。
I.(1) 醇类物质都含有的官能团是羟基,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(2) 三种醇与钠反应放出等量的氢气,三种醇提供的羟基数相等,设需要-OH的物质的量为nmol,而乙醇、乙二醇、甘油含有的羟基数分别为1:2:3,则三种醇的物质的量之比为nmol:![]() mol:
mol:![]() mol=6:3:2,故答案为:6:3:2;
mol=6:3:2,故答案为:6:3:2;
(3) 乙醇在铜作催化剂条件下氧化生成乙醛,化学方程式为2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O;反应类型为氧化反应,故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O;反应类型为氧化反应,故答案为:2CH3CH2OH+O2 ![]() 2CH3CHO+2H2O;氧化反应;
2CH3CHO+2H2O;氧化反应;
(4) 1mol丙三醇(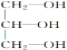 )与3mol乙酸分子脱去3mol水分子,发生酯化反应,方程式为:
)与3mol乙酸分子脱去3mol水分子,发生酯化反应,方程式为: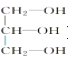 +3CH3COOH
+3CH3COOH![]()
 +3H2O,故答案为:
+3H2O,故答案为: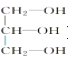 +3CH3COOH
+3CH3COOH![]()
 +3H2O;
+3H2O;
II.(5) 根据上述分析,A→B为硝基苯中间位上的氢原子被甲基取代的反应,化学反应方程式为: ![]() +CH3Cl
+CH3Cl ![]()
 +HCl;反应类型:取代反应,故答案为:
+HCl;反应类型:取代反应,故答案为:![]() +CH3Cl
+CH3Cl ![]()
 +HCl;取代反应;
+HCl;取代反应;
(6) C为溴苯,含有的官能团的名称为溴原子;D为4-溴苯磺酸,结构简式为![]() ,故答案为:溴原子;
,故答案为:溴原子;![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
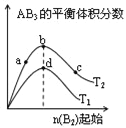
A. 图中T2一定大于T1
B. 图中b点速率一定大于d点速率
C. 达到平衡时,A2的转化率大小为:c>b>a
D. 加入催化剂可以使状态d变为状态b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用海水制盐工业中的母液来生产金属镁的一种工艺流程如下:

下列说法错误的是
A. 设计步骤①、②、③的主要目的是富集MgCl2
B. 脱水时在HCl气氛中进行可防止MgCl2发生水解
C. 电解得到的炽热镁粉不可在二氧化碳、氮气气氛中冷却
D. 上述工艺流程中涉及到的反应有置换反应、化合反应、复分解反应、分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。下列说法正确的是( )

A. 该装置将化学能转化为光能和电能
B. 该装置工作时,H+从b极区向a极区迁移
C. 每生成1molO2,有44g CO2被还原
D. a电极的反应为:3CO2+18H+-18e-=C3H8O+5H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置(部分夹持装置略去)进行相应的实验,能达到实验目的的是 ( )
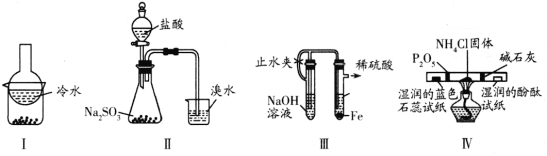
A. 加热装置I中的烧杯分离I2和高锰酸钾固体
B. 用装置II验证二氧化硫的漂白性
C. 用装置III制备氢氧化亚铁沉淀
D. 用装置IV检验氯化铵受热分解生成的两种气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化符合图示的是
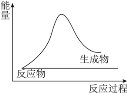
①冰雪融化②KMnO4分解制O2③铝与氧化铁的反应④钠与水反应⑤二氧化碳与灼热的木炭反应⑥碘的升华⑦Ba(OH)2·8H2O和NH4Cl的反应
A.②⑥⑦B.③④C.①②⑤⑥⑦D.②⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2SO2(g)+O2(g)![]() 2SO3(g)为放热反应,则下列说法正确的是
2SO3(g)为放热反应,则下列说法正确的是
A.单位时间内生成2molSO2,同时生成1molO2,说明反应达到平衡状态
B.上述热化学反应方程式说明反应物的总键能小于生成物的总键能
C.升高温度,正反应速率增大,逆反应速率减小
D.将2molSO2(g)和1molO2(g)置于一密闭容器中充分反应后生成2molSO3(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体吸入CO后在肺中发生反应CO+HbO2![]() O2+HbCO导致人体缺氧。向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L],氧合血红蛋白 HbO2浓度随时间变化曲线如图所示。下列说法正确的是( )
O2+HbCO导致人体缺氧。向某血样中通入CO与O2的混合气[c(CO)=1.0×10-4mol/L,c(O2)=9.9×10-4mol/L],氧合血红蛋白 HbO2浓度随时间变化曲线如图所示。下列说法正确的是( )

A.反应开始至4s内用HbO2表示的平均反应速率为2×l0-4mol/(L·s)
B.反应达平衡之前,O2与HbCO的反应速率逐渐减小
C.将CO中毒病人放入高压氧舱治疗是利用了化学平衡移动原理
D.该温度下反应CO+HbO2 ![]() O2+HbCO的平衡常数为107
O2+HbCO的平衡常数为107
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂、油漆调色、金属铋生产中,副产品 NaBiO3可作测定锰的氧化剂。工业上常用辉铋矿(主要成分是Bi2S3,还含有少量SiO2等杂质),制备BiOCl和NaBiO3(二者都难溶于水),其流程如下:
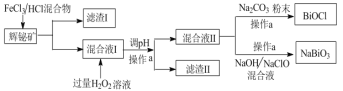
(1)操作a使用的玻璃仪器是_____________,工业上制备HCl的反应原理是:_____。
(2)滤渣I中的成分为________,分离滤渣I中的成分的物理方法是:__________。
(3)请从平衡角度解释调pH产生滤渣Ⅱ的原因:__。
(4)混合液 II 中加入 Na2CO3粉末,当混合液Ⅱ中____________(填实验现象)时,说明BiOCl的生成已完成。混合液II中加入NaOH和NaClO发生的离子方程式________。
(5)加入 H2O2发生反应的离子方程式_______,过滤后,如何洗涤BiOCl固体_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com