
A、B、C、D、E、F、G是原子序数依次增大的短周期元素,其中A与E、D与G同主族,且D与G核内质子数之和是A与E核内质子数之和的2倍,A与B、C、D可分别形成10电子分子,E、F、G元素最高价氧化物对应水化物之间可相互发生反应,请回答下列问题
(1)E、G两种元素的符号:E、G;F在元素周期表中的位置是 .
(2)Zn与稀硫酸反应需加入少量硫酸铜溶液反应速率会大大加快,其原理是 。
(3) E在D2中燃烧生成化合物X中阴阳离子个数比为 ;X中的阴离子电子式为 .
(4)能够说明可逆反应2CD2(g)  C2D4(g)达到平衡状态的标志是 ;
C2D4(g)达到平衡状态的标志是 ;
①单位时间消耗2mol CD2的同时,生成1 mol C2D4 ②恒温恒压下,混合气体的密度不变③CD2和C2D4的浓度之比为2∶1 ④混合气体的颜色不变⑤单位时间消耗4mol CD2的同时,消耗2mol C2D4
(5)向含E的最高价氧化物的水化物0.5 mol的水溶液中通入标况下BD2气体11.2L,其化学反应方程式为 。
(1) Na S 第三周期 ⅢA族
(2) 发生Zn+H2SO4=ZnSO4+Cu↓,形成铜锌原电池,反应速率加快;
(3)1∶2 略 (4)②④⑤ (5)NaOH+CO2 ==NaHCO3
【解析】
试题分析:根据题给信息推断,A为氢元素,B为碳元素,C为氮元素,D为氧元素,E为钠元素,F为铝元素,G为硫元素。(1)E为钠元素,G为硫元素,元素符号分别为:Na、S;F为铝元素,在元素周期表中的位置是第三周期 ⅢA族;(2)Zn与稀硫酸反应需加入少量硫酸铜溶液反应速率会大大加快,其原理是发生Zn+H2SO4=ZnSO4+Cu↓,形成铜锌原电池,反应速率加快;(3) 钠在O2中燃烧生成化合物过氧化钠中阴阳离子个数比为1∶2;过氧化钠中的阴离子电子式略;(4)①单位时间消耗2mol NO2的同时,生成1 mol N2O4 ,二者均为正反应速率,不能说明反应已达平衡,错误;②恒温恒压下,混合气体的密度随反应的进行不断变化,当混合气体的密度不变时,说明反应已达平衡状态,正确;③NO2和N2O4的浓度之比为2∶1 ,不能说明反应已达平衡,错误;④混合气体的颜色不变,二氧化氮的浓度不变,说明反应已达平衡状态,正确;⑤单位时间消耗4mol CD2的同时,消耗2mol C2D4,二者一个正反应速率,一个为逆反应速率,且速率之比等于化学计量数之比,说明反应已达平衡状态,正确;选②④⑤;(5)向氢氧化钠0.5 mol的水溶液中通入标况下CO2气体11.2L,其化学反应方程式为NaOH+CO2 ==NaHCO3。
考点:考查元素推断及相关物质的结构和性质。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2013-2014吉林省白城市高一上学期期末考试化学(A卷)试卷(解析版) 题型:选择题
下列说法正确的是( )
A.同温同压下,相同体积的物质,其物质的量一定相等
B.标准状况下气体摩尔体积约为22.4L
C.0.5 L 1 mol/L FeCl3溶液与0.2 L 1 mol/L KCl溶液中的Cl-的数目之比为15∶2
D.150 mL 1 mol/L NaCl溶液与50 mL 1 mol/L AlCl3溶液中Cl-物质的量浓度相等
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省高二5月月考化学试卷(解析版) 题型:推断题
有关物质间有下图所示的转化关系。其中:A的浓溶液与单质B在加热时才发生反应①;A的稀溶液与足量B发生反应②。据此填写下列空白:
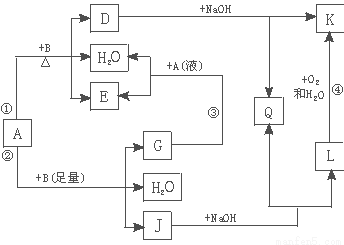
(1)反应④的现象是 。
(2)写出反应②的离子方程式 。
(3)根据题示信息判断,A的浓溶液和单质B加热时能否产生G,说明理由(写出化学方程式回答):
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省高二5月月考化学试卷(解析版) 题型:选择题
为了减少城市空气污染,要求使用无铅汽油,所谓无铅汽油是指( )
A.不用铅桶装的汽油 B.不含四乙基铅的汽油
C.不含Pb(NO3)2的汽油 D.不含氧化铅的汽油
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省高一下学期期末考试化学试卷(解析版) 题型:填空题
碱金属元素在科学研究与生产生活中有着非常广泛的用途。
(1)锂是最轻的金属,如果用锂做一架飞机,两个人就可以抬动。锂在元素周期表中的表示如图所示,填写以下空格。

①Li在元素周期表中的位置: 。
②6.941的意义: __________________________。
(2)光电管是利用碱金属铯受到光照射时能形成电流这一光电效应的性质制成的。
①完成铯的原子结构示意图:
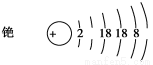
②下列有关铯的说法正确的是________。
A.其单质在常温下与水反应不如钠剧烈, B.其原子半径比钾原子半径小
C.其氢氧化物的水溶液不能使氢氧化铝溶解,D.其碳酸盐易溶于水
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省高一下学期期末考试化学试卷(解析版) 题型:实验题
(1)小明在做“研究温度对反应速率的影响”实验时,他取了两只试管,均加入4mL 0.01mol/L的KMnO4酸性溶液和2mL 0.1mol/L H2C2O4(乙二酸)溶液,振荡,A试管置于热水中,B试管置于凉水中,记录溶液褪色所需的时间。
①需要用 来酸化KMnO4溶液,褪色所需时间tA tB(填“>”、“=”或“<”).
②写出该反应的离子方程式 .
(2)实验室有瓶混有泥沙的乙二酸样品,小明利用这个反应的原理来测定其含量,具体操作为:
①配制250mL溶液:准确称量5.0g乙二酸样品,配成250mL溶液。
②滴定:准确量取25.00mL所配溶液于锥形瓶中,加少量酸酸化,将0.1000mol?L﹣1KMnO4溶液装入
(填“酸式”或“碱式”)滴定管,进行滴定操作。在实验中发现,刚滴下少量KMnO4溶液时,溶液迅速变成紫红色。将锥形瓶摇动一段时间后,紫红色慢慢消失;再继续滴加时,紫红色就很快褪色了。请解释原因: 。当 ,证明达到滴定终点.
③计算:再重复上述操作2次,记录实验数据如下.
序号 | 滴定前读数(mL) | 滴定后读数(mL) |
1 | 0.00 | 20.10 |
2 | 1.00 | 20.90 |
3 | 0.00 | 21.10 |
则消耗KMnO4溶液的平均体积为 mL,已知H2C2O4的相对分子质量为90,则此样品的纯度为 。
④误差分析:下列操作会导致测定结果偏高的是 。
A.未用标准浓度的酸性KMnO4溶液润洗滴定管
B.滴定前锥形瓶有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.不小心将少量酸性KMnO4溶液滴在锥形瓶外
E.观察读数时,滴定前仰视,滴定后俯视.
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列实验操作或对实验事实的描述正确的是( )
A.欲将蛋白质从水中析出而又不改变它的性质,应加入CuSO4溶液
B.乙醇可以被氧化为乙酸,二者都能发生酯化反应
C.淀粉溶液中加入一定量稀硫酸,共热一段时间后,向溶液中加入新制氢氧化铜悬浊液并加热煮沸,未见红色固体产生,证明淀粉没有发生水解
D.可用NaOH溶液除去混在乙酸乙酯中的乙酸
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省高一5月月考化学试卷(解析版) 题型:选择题
下列说法正确的是 ( )
A.淀粉和蛋白质均可作为生产葡萄糖的原料
B.实验室可用酸性高锰酸钾溶液鉴别甲苯和己烯
C.石油裂化和油脂皂化都是高分子生成小分子的过程
D.装饰材料中的甲醛和芳香烃会造成居室污染
查看答案和解析>>
科目:高中化学 来源:2013-2014吉林省下学期期中考试高一化学试卷(解析版) 题型:计算题
写出下列物质的电子式,有结构式的请写出结构式
①氨气 、 ②氯化铵 、
③干冰 、 ④苛性钠 、
⑤冰 、 ⑥过氧化钠 、
⑦双氧水 、 ⑧HClO 、
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com