
| A、电解时,石墨作阳极,铁作阴极 |
| B、阴极的电极反应式为:2H++2e-═H2↑ |
| C、电解过程中阳极周围溶液的pH变大 |
| D、理论上每生成1mol KIO3则电路中流过6mol电子 |
| ||
| ||


科目:高中化学 来源: 题型:
| A、HCl、CuSO4、Mg(NO3)2、KOH |
| B、NaBr、AgNO3、HCl、Na2CO3 |
| C、H2SO4、NaCl、Na2SO4、Na2CO3 |
| D、NaOH、MgSO4、Na2CO3、KHSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
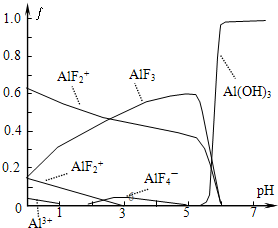 氟和氟盐是化工原料.由于氟气性质活泼,很晚才制取出来.
氟和氟盐是化工原料.由于氟气性质活泼,很晚才制取出来.查看答案和解析>>
科目:高中化学 来源: 题型:
- 3 |
2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaOH、H2SO4、Na2SO4 |
| B、NaOH、AgNO3、H2SO4 |
| C、HCl、CuBr2、Ba(OH)2 |
| D、KBr、H2SO4、Ba(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将固体加入容量瓶中溶解并稀释至刻度,配置成一定物质的量浓度的溶液 |
| B、某溶液与BaCl2溶液反应生成白色沉淀,说明原溶液中有SO42- |
| C、用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 |
| D、可以用湿润的红色石蕊试纸检验是否有氨气生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| t/s | 0 | 5 | 15 | 25 | 35 |
| n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A、反应在前5s的平均速率v(A)=0.03mol?L-1?s-1 |
| B、保持其他条件不变,升高温度,平衡时c(A)=0.41mol?L-1,则反应的△H>0 |
| C、相同温度下,起始时向容器中充入2.0mol C,达到平衡时,C的转化率大于80% |
| D、相同温度下,起始时向容器中充入0.40mol A、0.40mol B和0.10mol C,反应达到平衡前v(正)<v(逆) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com