
分析 (1)①F元素为-1价,根据化合物中化合价的代数和为零计算;
②将Fz通入稀的NaOH溶液中可得到OF2、NaF和水;
(2)①A.亚硝酸钠是强碱弱酸盐其水溶液呈碱性,氯化钠是强酸强碱盐其水溶液呈中性;
B.甲基橙的变色范围是3.1-4.4;
C.酸性条件下,亚硝酸根离子能被碘离子还原生成一氧化氮,同时生成碘单质;
D.亚硝酸根离子不和银离子反应,氯离子和银离子反应生成白色沉淀;
②Cl2、HNO3都能氧化亚铁离子,但能引入新的杂质,铁不能氧化亚铁离子,双氧水的还原产物是水,不引入杂质.
③把酸性高锰酸钾溶液滴入到NaNO2溶液中,观察到紫色褪色,同时生成NO3-和Mn2+,二者发生氧化还原反应;
④高铁酸钾具有氧化性可以消毒杀菌,在水中被还原为三价铁离子,三价铁离子水解生成氢氧化铁胶体具有吸附悬浮杂质的作用.
解答 解:(1)①F元素为-1价,化合物中化合价的代数和为零,则OF2中O为+2价,故答案为:+2;
②将Fz通入稀的NaOH溶液中可得到OF2、NaF和水,其反应方程式为:2F2+2NaOH=2NaF+H2O+OF2,故答案为:2F2+2NaOH=2NaF+H2O+OF2;
(2)①A.亚硝酸钠是强碱弱酸盐其水溶液呈碱性,氯化钠是强酸强碱盐其水溶液呈中性,相同物质的量浓度的两种溶液的pH不同,所以可以用测定这两种溶液的pH值鉴别,故A不选;
B.亚硝酸钠是强碱弱酸盐其水溶液呈碱性,氯化钠是强酸强碱盐其水溶液呈中性,甲基橙的变色范围是3.1-4.4,所以亚硝酸钠和氯化钠溶液加入甲基橙后溶液都呈黄色,反应现象相同,所以不能用甲基橙鉴别,故B选;
C.在酸性条件下,亚硝酸钠和碘离子反应方程式为2NO2-+2I-+4H+=2NO↑+I2+2H2O,碘遇淀粉变蓝色,氯离子和碘离子不反应,所以反应现象不同,所以可以用酸性条件下的KI淀粉试液来区别,故C不选;
D.亚硝酸根离子不和银离子反应,氯离子和银离子反应生成不溶于硝酸的白色沉淀,反应现象不同,所以可以用AgNO3和HNO3两种试剂来区别,故D不选;
故答案为:B;
②由于Cl2、HNO3都能氧化亚铁离子,但能引入新的杂质,铁不能氧化亚铁离子,双氧水的还原产物是水,不引入杂质,所以正确是双氧水,
故答案为:C.
③酸性高锰酸钾溶液滴入到NaNO2溶液中,观察到紫色褪色,同时生成NO3-和Mn2+,反应的离子方程式为:6H++5NO2-+2MnO4-═NO3-+2Mn2++3H2O;
故答案为:6H++5NO2-+2MnO4-═NO3-+2Mn2++3H2O;
④高铁酸钾( K2FeO4)中Fe的化合价是+6价,具有强氧化性,能杀菌消毒,其还原产物Fe3+水解生成氢氧化铁胶体,能吸附水中杂质,所以高铁酸钾作为水处理剂发挥的作用是净水、消毒,
故答案为:净水、消毒.
点评 本题考查综合考查了OF2、亚硝酸盐、铁盐的性质,涉及了化学方程式的配平、高铁酸钾的净水、消毒原理,为高频考点,侧重于学生的分析能力的考查,注意二价铁离子和三价铁离子的检验是高考的热点,注意相关基础知识的积累,题目难度中等


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
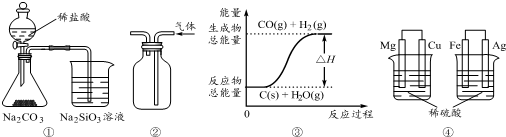
| A. | 用图①所示实验可比较氯、碳、硅三种元素的非金属性强弱 | |
| B. | 用图②所示实验装置排空气法收集NO2气体 | |
| C. | 图③表示可逆反应C(s)+H2O(g)?CO(g)+H2(g)的△H小于0 | |
| D. | 图④两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
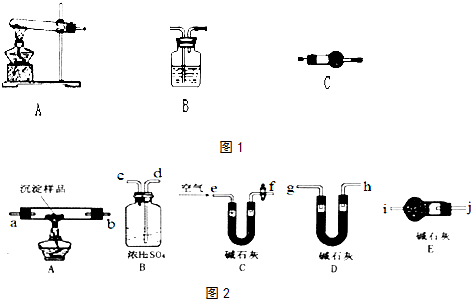
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 阳离子 | K+ NH4+ Fe2+ Mg2+ Al3+ Cu2+ |
| 阴离子 | OH- Cl- Al02- CO32- SiO32-SO42- |
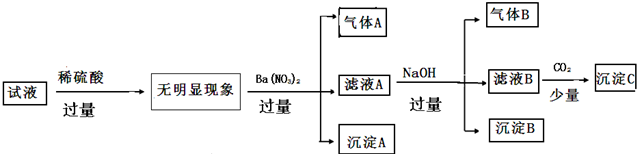
| A. | 原溶液中只含有NH4+ Fe2+Cl- SO42- | |
| B. | 由沉淀A推断原溶液中一定含有SO42- | |
| C. | 滤液A中可能含有K+ Al3+ Cl- | |
| D. | 沉淀B中一定含有Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +3 | B. | +1 | C. | +4 | D. | +2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=7的溶液 | |
| B. | 氨水和硫酸铵的混合液中c(NH4+)=2c(SO42-) | |
| C. | c(H+)=10-7 mol•L-1的溶液 | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=10-14的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com