
| A. | ④⑤⑥ | B. | ①②③④ | C. | ①②④⑥ | D. | ②③④ |
分析 A.利用⑤可计算质量分数,再利用c=$\frac{1000ρω}{M}$计算出该溶液的物质的量浓度;
B.根据①②可计算溶质的质量,再由④计算溶质的物质的量,然后根据③及c=$\frac{n}{V}$计算出溶液的浓度;
C.②⑥可以计算溶液体积,①④可以计算溶质的物质的量,再根据c=$\frac{n}{V}$计算溶液物质的量浓度;
D.无法计算溶质的物质的量.
解答 解:A.利用⑤可计算质量分数,再由④、⑥并结合c=$\frac{1000ρω}{M}$可计算该饱和溶液物质的量浓度,故A正确;
B.根据“①溶液的质量、②溶剂的质量”可计算溶质的质量,再由④及n=$\frac{m}{M}$计算溶质的物质的量,由③及c=$\frac{n}{V}$可计算这种饱和溶液物质的量浓度,故B正确;
C.②⑥可以计算溶液体积,①④可以计算溶质的物质的量,再根据c=$\frac{n}{V}$计算溶液物质的量浓度,故C正确;
D.无法计算溶质的物质的量,所以无法计算溶液物质的量浓度,故D错误;
故选D.
点评 本题考查物质的量浓度的计算,题目难度中等,注意掌握物质的量浓度的概念及计算方法,熟悉物质的量浓度的计算公式及各个量之间的关系是解答本题的关键,侧重考查学生对各个公式的理解和运用,题目难度不大.


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
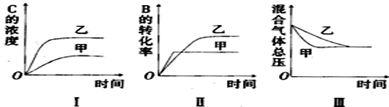
| A. | 图I研究的可能是不同催化剂对反应的影响,且乙使用的催化剂效率较高 | |
| B. | 图Ⅱ研究的可能是压强对反应的影响,且甲的压强较高 | |
| C. | 图Ⅱ研究的可能是温度对反应的影响,且甲的温度较高 | |
| D. | 图Ⅲ研究的可能是不同催化剂对反应的影响,且乙使用的催化剂效率较高 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
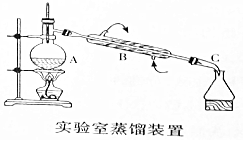 如图是用自来水制备蒸馏水的实验装置图.
如图是用自来水制备蒸馏水的实验装置图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol | B. | 0.5 mol | C. | 0.75 mol | D. | 0.25 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(OH)2 溶液 | B. | 饱和NaCl溶液 | C. | 自来水 | D. | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原反应中,一种元素被氧化,一定是另一种元素被还原 | |
| B. | 某元素由化合态变成游离态,此元素可能被氧化,也可能被还原 | |
| C. | 金属单质在反应中只能作还原剂,非金属单质只能作氧化剂 | |
| D. | 金属原子失电子越多,其还原性越强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将集有氨气的试管倒扣于水槽中,液体迅速充满试管,说明氨气极易溶于水 | |
| B. | 将湿润的红色石蕊试纸放入集有氨气的集气瓶中,试纸由红色变为蓝色,说明氨水呈碱性 | |
| C. | 加热NH4HCO3固体,观察到固体逐渐减少,试管口有液滴产生,说明NH4HCO3受热不稳定 | |
| D. | 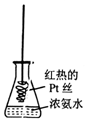 将红热的Pt丝伸入如图所示的锥形瓶中,瓶口出现少量红棕色气体,说明氨气的直接氧化产物为NO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com