
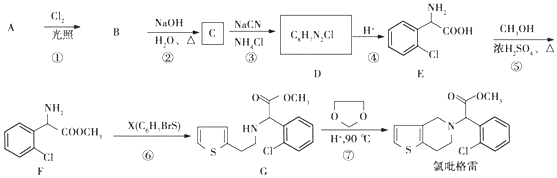
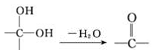 ;②
;②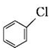 中氯原子较难水解;③RCHO$→_{NH_{4}Cl}^{NaCN}$
中氯原子较难水解;③RCHO$→_{NH_{4}Cl}^{NaCN}$
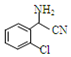 ;C分子中最多有14个原子共平面.
;C分子中最多有14个原子共平面.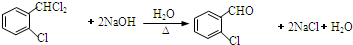 .
. ,需要经历的反应类型有②①③④③(填写编号).①加成反应 ②消去反应 ③取代反应 ④氧化反应 ⑤还原反应,写出制备化合物
,需要经历的反应类型有②①③④③(填写编号).①加成反应 ②消去反应 ③取代反应 ④氧化反应 ⑤还原反应,写出制备化合物 的最后一步反应HOCH2CH2OH+HCHO$\stackrel{酸}{→}$
的最后一步反应HOCH2CH2OH+HCHO$\stackrel{酸}{→}$ .
.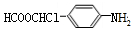 .
.分析 (1)(2)(3)根据D的分子式及E的结构简式可知,D为 ,根据信息③可知C为
,根据信息③可知C为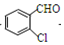 ,根据相互转化关系,A与氯气发生取代生成B,B水解得C,所以A为
,根据相互转化关系,A与氯气发生取代生成B,B水解得C,所以A为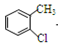 ,B为
,B为 ,
,
(4)由乙醇、甲醇为有机原料制备化合物 ,可以用乙醇发生消去反应生成乙烯,乙烯与溴发生加成反应生成1,2-二溴乙烷,再发生水解反应生成乙二醇,甲醇催化氧化生成HCHO,最后乙二醇与甲醛反应生成
,可以用乙醇发生消去反应生成乙烯,乙烯与溴发生加成反应生成1,2-二溴乙烷,再发生水解反应生成乙二醇,甲醇催化氧化生成HCHO,最后乙二醇与甲醛反应生成 ,
,
(5)①结构中含有苯环且存在与F相同的官能团,即含有酯基、氨基、氯原子;②能发生银镜反应,其碱性条件下水解的两种产物也能发生银镜反应,则应为甲酸某酯,且氯原子应连在酯基中醇的碳上,结合E的结构简式书写同分异构体,据此答题.
解答 解:(1)A为 ,A的名称是邻氯甲苯,根据F的结构简式可知,F中无氧官能团的名称是氨基和氯原子,
,A的名称是邻氯甲苯,根据F的结构简式可知,F中无氧官能团的名称是氨基和氯原子,
故答案为:邻氯甲苯;氨基和氯原子;
(2)根据上面的分析可知,D为 ,C为
,C为 ,C分子中最多有14个原子共平面,
,C分子中最多有14个原子共平面,
故答案为: ;14;
;14;
(3)反应②为卤代烃在NaOH溶液中水解,生成2个羟基,脱水生成醛基,化学方程式为 ,
,
故答案为: ;
;
(4)由乙醇、甲醇为有机原料制备化合物 ,可以用乙醇发生消去反应生成乙烯,乙烯与溴发生加成反应生成1,2-二溴乙烷,再发生水解反应生成乙二醇,甲醇催化氧化生成HCHO,最后乙二醇与甲醛反应生成
,可以用乙醇发生消去反应生成乙烯,乙烯与溴发生加成反应生成1,2-二溴乙烷,再发生水解反应生成乙二醇,甲醇催化氧化生成HCHO,最后乙二醇与甲醛反应生成 ,所以需要经历的反应类型有消去反应、加成反应、取代反应、氧化反应、取代反应,制备化合物
,所以需要经历的反应类型有消去反应、加成反应、取代反应、氧化反应、取代反应,制备化合物 的最后一步反应为HOCH2CH2OH+HCHO$\stackrel{酸}{→}$
的最后一步反应为HOCH2CH2OH+HCHO$\stackrel{酸}{→}$ ,
,
故答案为:②①③④③;HOCH2CH2OH+HCHO$\stackrel{酸}{→}$ ;
;
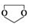
(5)根据E的结构简式,结合条件①结构中含有苯环且存在与F相同的官能团,即含有酯基、氨基、氯原子;②能发生银镜反应,其碱性条件下水解的两种产物也能发生银镜反应,则应为甲酸某酯,且氯原子应连在酯基中醇的碳上,则符合条件的结构为苯环上连有两个基团为HCOOCHCl-、-NH2,有3种结构,其中一种的核磁共振氢谱显示5组峰,且峰面积之比为1:1:2:2:2,其结构简式为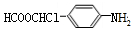 ,
,
故答案为:3;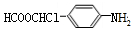 .
.
点评 本题考查有机物推断与合成,侧重考查学生分析推断及知识迁移能力,为高考高频点,能根据流程图中结构简式变化方式判断反应类型,难点是(4)中的合成路线的分析,题目难度中等.


 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:选择题
| A. | CuSO4 | B. | NaCl | C. | CaCl2 | D. | 无 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
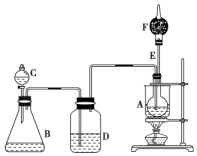 已知CH3CH2OH+NaBr+H2SO4CH3CH2Br+NaHSO4+H2O,如图是某校化学课外活动小组设计的乙醇与氢卤酸反应的实验装置图.
已知CH3CH2OH+NaBr+H2SO4CH3CH2Br+NaHSO4+H2O,如图是某校化学课外活动小组设计的乙醇与氢卤酸反应的实验装置图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
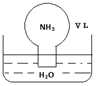 标准状况下,将体积为V L充满氨气的圆底烧瓶倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出,所得溶液的密度为ρg•cm-3.下列说法错误的是( )
标准状况下,将体积为V L充满氨气的圆底烧瓶倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出,所得溶液的密度为ρg•cm-3.下列说法错误的是( )| A. | 水最终会充满整个烧瓶 | |
| B. | 所得溶液的物质的量浓度为 $\frac{1}{22.4}$mol•L-1 | |
| C. | 所得溶液的质量分数为$\frac{17}{22400}$ρ | |
| D. | 将氨气换为二氧化氮,所得溶液的物质的量浓度也为$\frac{1}{22.4}$mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制100g20%的氢氧化钠溶液(烧杯、100mL容量瓶、胶头滴管) | |
| B. | 钠的焰色反应(铂丝、硫酸钠溶液、稀盐酸) | |
| C. | 从碘水中提取碘(蒸发皿、酒精灯、玻璃棒) | |
| D. | 除去自来水中的Cl-(铁架台、玻璃棒、漏斗) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com