
| A. | 放电时,蓄电池由化学能转化为电能 | |
| B. | 充放电时,溶液的导电能力变化不大 | |
| C. | 放电时的负极反应式为 Pb-2e-═Pb2+ | |
| D. | 充电时的阳极反应式为 Pb2++4OH-+2e-═PbO2+2H2O |
分析 在充电时,该装置是电解池,阳极失电子发生氧化反应,阴极上得电子发生还原反应;放电时,该装置是原电池,负极上铅失电子发生氧化反应,正极上二氧化铅得电子发生还原反应,酸参加反应,根据充放电时,两极上的电极反应来回答.
解答 解:在充电时,该装置是电解池,阳极上甲基磺酸铅失电子发生氧化反应,即Pb2++2H2O-2e-=PbO2+4H+,阴极上甲基磺酸铅得电子发生还原反应,放电时,该装置是原电池,负极上铅失电子发生氧化反应,即Pb-2e-=Pb2+,正极上二氧化铅得电子发生还原反应,即PbO2+4H++2e-=Pb2++2H2O.
A.放电时是原电池的工作原理,蓄电池由化学能转化为电能,故A正确;
B.充放电时,溶液的电荷浓度几乎不发生变化,导电能力不变化,故B正确;
C.负极上铅失电子发生氧化反应,电极反应式为:Pb-2e-=Pb2+,故C正确;
D.充电时的阳极Pb2+失去电子发生氧化反应,正确的电极反应式为:Pb2++2H2O-2e-=PbO2+4H+,故D错误;
故选D.
点评 本题考查原电池、电解池工作原理及应用,题目难度不大,注意原电池和电解池的工作原理知识的灵活应用,正确判断两极为解答关键,试题侧重考查学生的分析、理解能力及灵活应用能力.


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:推断题
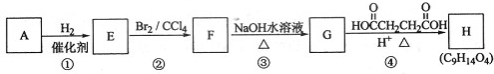
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为测定新制氯水的pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| B. | 热的浓盐酸可以除去试管内残留的MnO2 | |
| C. | 在未知溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在SO42-或SO32- | |
| D. | 施肥时,草木灰(有效成分为K2CO3)与NH4Cl混合使用,可以同时提供K、N两种有效成分 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
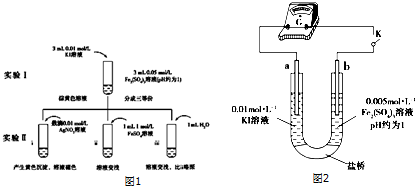
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
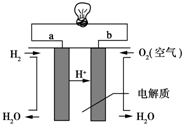 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ,属于加聚反应(填反应类型).
,属于加聚反应(填反应类型).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
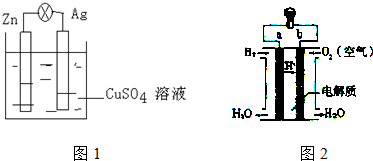
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com