
【题目】污水处理厂处理含CN-废水的过程分两步进行:①向含CN-的废水中加入过量NaC1O将CN-转化为CNO-;②调节①所得溶液为酸性,使CNO-继续被NaC1O转化为两种无污染的气体。下列关于上述过程的叙述错误的是( )
A.CN-的电子式为![]()
B.过程①中,生成CNO-的反应中氧化剂与还原剂的物质的量之比为1:1
C.过程②中,生成的两种无污染的气体为CO2和N2
D.氧化性:CNO->C1O-
科目:高中化学 来源: 题型:
【题目】某同学设计的微型实验装置验证SO2的性质,通过分析实验,下列结论表达正确的是
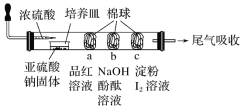
A. a棉球褪色,验证SO2具有氧化性
B. b棉球褪色,验证SO2具有酸性氧化物的通性
C. c棉球蓝色褪去,验证SO2漂白性
D. 可以使用浓硫酸吸收尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述中不正确的是
A. 25℃,pH=13的Ba(OH)2溶液中OH-数目为0.1NA
B. 常温常压下,22.4L Cl2和5.6gFe充分反应转移电子数目为0.3 NA
C. 8.0gCu2S和CuO的混合物中所含的铜原子数为0.1 NA
D. 标准状况下,5.6L乙烷中含有的极性键数目为1.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把6.5gZn放入足量的盐酸中,锌完全反应。计算:
(1)6.5gZn的物质的量?_________。
(2)参加反应的HCl的物质的量?_________。
(3)生成氢气的体积(标准状况)?__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向200mL FeBr2溶液中逐渐通入C12,其中n(Fe3+)、n(Br2)随通入n(Cl2)的变化如图所示,下列说法不正确的是( )

A.氧化性强弱:Br2>Fe3+
B.由图可知,该FeBr2溶液的浓度为1molL─1
C.n(Cl2)= 0.12 mol时,溶液中的离子浓度有c(Fe3+):c(Br-)=1:8
D.c(FeBr2):c(Br2)= 1: 1时,反应的离子方程式:2Fe3++2Br-+2Cl2=2Fe3++Br2+4Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:电流效率=电路中通过的电子数÷消耗负极材料失去电子总数。现有三个电池装置如图所示:
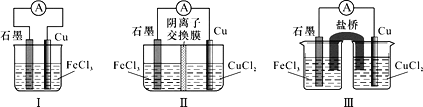
下列说法正确的是
A.Ⅰ、Ⅱ和Ⅲ的电池反应均为:Cu+Fe3+=Cu2++Fe2+
B.Ⅲ中烧杯里的Cl-从右池经过盐桥移向左池
C.5min后,Ⅰ、Ⅱ和Ⅲ中都只含两种溶质
D.Ⅱ、Ⅲ的电流效率均高于Ⅰ的电流效率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解足量下列溶液一段时间后,再加入一定量括号内的纯净物,能使溶液恢复到原来的成分和浓度的是
A. AgNO3[AgNO3] B. NaOH[NaOH] C. KCl[H2O] D. CuSO4[CuO]
【答案】D
【解析】石墨电极为惰性电极,溶液中阳离子在阴极放电,阴离子在阳极放电。A、电解AgNO3溶液,Ag+在阴极放电生成Ag,OH-在阳极放电生成O2,且n(Ag)∶n(O2)=2∶1,则应加入Ag2O恢复浓度,故A错误;B、电解NaOH溶液,H+在阴极放电生成H2,OH-在阳极放电生成O2,且n(H2)∶n(O2)=2∶1,则应加入一定量的H2O恢复原样,故B错误;C、电解KCl溶液,H+在阴极放电生成H2,Cl-在阳极放电生成Cl2,且n(H2)∶n(Cl2)=1∶1,则应加入一定量HCl恢复原样,故C错误;D、电解CuSO4溶液,Cu2+在阴极放电生成Cu,OH-在阳极放电生成O2,且n(Cu)∶n(O2)=2∶1,则应加入一定量CuO恢复原样,故D正确。故选D。
点睛:分析电解反应的原理,在两极析出什么物质(固体或气体),相当于什么物质脱离反应体系,根据元素守恒和原子比例,加入对应的物质,即可使溶液完全复原。
【题型】单选题
【结束】
28
【题目】工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的是

已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A. 碳棒上发生的电极反应:4OH--4e-=O2↑+2H2O
B. 电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C. 为了提高Ni的产率,电解过程中需要控制废水pH
D. 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将甲烷与氯气按1:3的体积比混合于一试管中,倒立于盛有饱和食盐水的水槽,置于光亮处(如图所示),下列有关此实验的现象和结论的叙述不正确的是( )
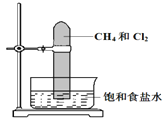
A. 试管中气体的黄绿色逐渐变浅,水面上升
B. 生成物只有三氯甲烷和氯化氢在标准状况下是气体
C. 试管内壁有油状液滴形成
D. 试管内有少量白雾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某天然氨基酸M是人体必需的氨基酸之一,其合成路线如下:
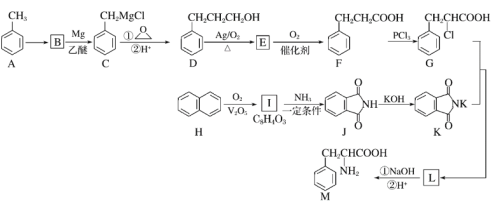
已知:
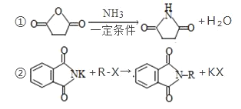
回答下列问题:
(1)A→B的反应条件和试剂是___________,反应类型是_______________。
(2)化合物M的名称为_________________,其含有_______________个手性碳原子。
(3)写出D→E反应的化学方程式:___________________。
(4)I与乙二醇反应可生成能降解的高分子化合物N,写出该反应的化学方程式:___________________。
(5)符合下列条件的化合物M的同分异构体共有____________种(不考虑立体异构),其中核磁共振氢谱峰面积比为1∶1∶2∶2∶2∶3的分子的结构简式:______________(任写一种)。
①含有苯甲酸结构 ②含有一个甲基 ③苯环上只有两个取代基
(6)L与NaOH反应的化学方程式为______________________。
(7)请结合以上合成路线,写出以丙酸和上述流程中出现的物质为原料经三步合成丙氨酸(![]() )的路线_______。
)的路线_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com