
| A. | 化学反应中的能量变化,通常表现为热量的变化 | |
| B. | 反应物的总能量高于生成物的总能量时发生放热反应 | |
| C. | Ba(OH)2•8H2O与NH4Cl的反应是吸热反应 | |
| D. | 一氧化碳在氧气中的燃烧是吸热反应 |
分析 化学反应中的能量变化,通常表现为热量的变化.如果反应物所具有的总能量高于生成的总能量,则在反应中会有一部分能量转变为热能的形式释放,这就是放热反应,反之则是吸热反应,并注意反应条件与反应吸热、放热无关.
解答 解:A、化学反应中的能量变化通常表现为热量的变化,有时以热能、光能、电能等形式转化,故A正确;
B、当反应物的总能量高于生成物的总能量时,反应物的能量过剩,故为放热反应,故B正确;
C、Ba(OH)2•8H2O与NH4Cl的反应中反应物的总能量小于生成物的总能量,故是吸热反应,故C正确;
D、所有物质的燃烧均为放热反应,故CO的燃烧为放热反应,故D错误.
故选D.
点评 本题考查化学反应中的能量变化.化学反应中的能量变化通常表现为热量的变化.


 星级口算天天练系列答案
星级口算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 一小块钠投入水中:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 用氢氧化钠溶液吸收过量二氧化碳 OH-+CO2═HCO3- | |
| D. | Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 为了增强其氧化性,在配制时加入一定浓度的盐酸 | |
| B. | 该物质在反应中可以被还原,也可以被氧化 | |
| C. | 可用酸化的KMnO4溶液可以鉴别甲烷和乙烯 | |
| D. | KMnO4中Mn元素为其最高价+7,故含有最高价元素的化合物,均有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中Na+浓度增大,有H2放出 | |
| B. | 溶液中Na+数目减少,有H2放出 | |
| C. | 溶液中Na+与OH-浓度都增大,有H2放出 | |
| D. | 溶液中OH-数目增大,有H2放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
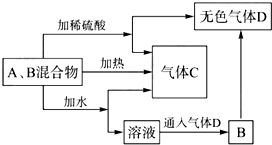 有A、B两种常见化合物,其焰色反应均呈黄色,C是一种单质气体,相互转化关系如图所示(其他物质均已略去).回答下列问题:
有A、B两种常见化合物,其焰色反应均呈黄色,C是一种单质气体,相互转化关系如图所示(其他物质均已略去).回答下列问题:
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
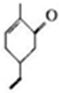 .下列有关M的说法正确的是( )
.下列有关M的说法正确的是( )| A. | 可以发生氧化反应 | B. | 分子式C9H10O | ||
| C. | 分子中所有原子都处子同一平面上 | D. | 不能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com