
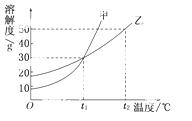
甲、乙两物质的溶解度曲线如图所示.下列叙述中,正确的是  ( )
( )
 A.t1℃时
A.t1℃时 ,在100 g水中放入60 g甲,其溶质的质量分数为37.5%
,在100 g水中放入60 g甲,其溶质的质量分数为37.5%
B.t1℃时,甲和乙的饱和溶液的物质的量浓度一定相等
C.t2℃时,甲和乙的饱和溶液中溶质的质量分数一定相等
D.t2℃时,分别在100 g水中各溶解20 g甲、乙,同时降低温度,
甲先达到饱和
科目:高中化学 来源: 题型:
汽车尾气里含有的NO气体是由内燃机燃烧时产生的高温引起氮气和氧气反应所致:N2(g)+O2(g) 2NO(g)
2NO(g) 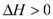
已知该反应在 2404℃时,平衡常数 K=6.4×10-3。请回答下列问题。
(1)该反应的平衡常数表达式为 。
(2)该温度下,向 2 L 密闭容器中充入 N2 和 O2 各 1 mol,平衡时,N2 的转化率是 %(保留整数)。
(3)该温度下,某时刻测得容器内 N2、O2、NO的浓度分别为2.5×10-1mol·L-1、4.0×10-2mol·L-1和3.0×10-3mol·L-1,此时反应________(填“处于化学平衡状态”、“向正方向进行”或“向逆方向进行”),理由是_______。
(4)将 N2、O2 的混合气体充入恒温恒容密闭容器中,如图变化趋势正确的是_________。
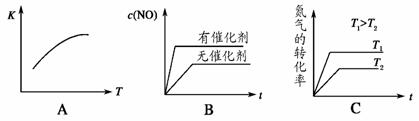
(5)向恒温恒容的密闭容器中充入等物质的量的 N2 和 O2,达到平衡状态后再向其中充入一定量 NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数_________(填“变大”、“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
100.0 mL 6.0 mol·L-1H2SO4溶液跟足量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不
影响生成H2的总量,可向反应物中加入适量的( )
A.Na2CO3(s) B.水
C.CuSO4(aq) D.NaHSO4(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知汽车尾气无害化处理反应为2NO(g)+2CO(g)  N2(g)+2CO2(g)。下列说法
N2(g)+2CO2(g)。下列说法
不正确的是 ( )
A.升高温度可使该反应的逆反应速率降低
B.使用高效催化剂可有效提高正反应速率
C.反应达到平衡后,NO的反应速率保持恒定
D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
在1.0 L密闭容器中放入0.10molA(g),在一定温度进行如下反应应:
A(g) B(g)+C(g) △H=+85.
B(g)+C(g) △H=+85. 1kJ·mol-1
1kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
| 时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 总压强p/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为 。
(2)由总压强P和起始压强P0计算反应物A的转化率α(A)的表达式为 。
平衡时A的转化率为 ,列式并计算反应的平衡常数K 。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总= mol,n(A)= mol。
②下表为反应物A浓度与反应时间的数据,计算a=
| 反应时间t/h | 0 | 4 | 8 | 16 |
| C(A)/(mol·L-1) | 0.10 | a |
| 0.0065 |
分析该反应中反应反应物的浓度c(A)变化与时间间隔(△t)的规律,得出的结论是 ,
由此规律推出反应在12h时反应物的浓度c(A)为 mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
有Na2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的物质的量浓度为0.4 mol/L,SO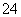 的物质的量浓度为0.7 mol/L,则此溶液中Na+的物质的量浓度为 ( )
的物质的量浓度为0.7 mol/L,则此溶液中Na+的物质的量浓度为 ( )
A.0.1 mol/L B.0.15 mol/L
C.0.2 mol/L D.0.25 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中,错误的是( )
A.配制5%食盐溶液时,将称量的食盐放入烧杯中加适量的水搅拌溶解
B.硫酸铜结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅
C.测定未知NaOH溶液浓度时,酸式滴定管需用标准酸 液润洗2~3次
液润洗2~3次
D.配制0.1 mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量 瓶中加水稀释
瓶中加水稀释
查看答案和解析>>
科目:高中化学 来源: 题型:
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是
A.若M(甲)<M(乙),则气体的压强:甲>乙
B.若M(甲)>M(乙),则气体的摩尔体积:甲<乙
C.若M(甲)>M(乙),则气体体积:甲<乙
D.若M(甲)<M(乙),则分子数:甲<乙
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下可逆反应N2+3H2  2NH3已达到平衡,
2NH3已达到平衡,
下列有关说法正确的 ( )
① 1个N≡N键断裂的同时,有3个H—H键形成 ② 反应混合物中各组分的体积分数保持不变
③ 恒温恒容时,容器内的压强不再改变 ④ 1个N≡N键断裂的同时,有3个N—H 键形成
⑤ NH3生成的速率与NH3分解的速率相等 ⑥ 单位时间生成n molN2,同时生成2n molNH3
⑦ 气体的平均相对分子质量不再改变 ⑧ N2 H2 NH3的分子数一定为1∶3∶2
⑨ 恒温恒容时,气体的总物质的量不再改变 ⑩ 恒温恒压时,容器内的密度不再改变
A.①②③④⑤⑥⑦⑨ B.①②③⑤⑥⑩ C. ③④⑤⑥⑦ ⑧ D.①②③⑤⑥⑦⑨⑩
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com