
【题目】氮在自然界中的转化是一个复杂的过程,涉及到地球上生物的方方面面。
(1)下列关于自然界中氮循环(如下图)的说法不正确的是(______)

A.氮元素均被氧化
B.工业合成氨属于人工固氮
C.含氮无机物和含氮有机物可相互转化
D.碳、氢、氧三种元素也参与了氮循环
(2)汽车尾气中的NO和NO2,是大气污染的物质。
①写出NO造成酸雨的两个化学反应方程式____________________。
②在汽车尾气排放管中安装一个催化转化器,可将尾气中另一种有害气体CO跟NO反应转化为无毒气体,该反应的化学反应方程式______________________________。
③用O2-NaOH吸收法可以除去烟道气中的NO2。反应的化学方程式是______________________________。
(3)用化学方程式表达工业上以NH3为原料生产HNO3的第一步______________________________。
【答案】 A 2NO+O2=2NO23NO2+H2O=2HNO3+NO 2NO+2CO=N2+2CO2 4NO2+O2+4NaOH=4NaNO3+2H2O 4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
【解析】(1)A.硝酸盐中氮元素的化合价为+5价,被细菌分解变成大气中氮单质,氮元素由+5→0,属于被还原,故A错误;B.工业合成氨是将N2与H2在一定条件下反应生成NH3,属于人工固氮,故B正确;C.氮循环中铵盐和蛋白质可相互转化,铵盐属于无机物,蛋白质属于有机物,含氮无机物和含氮有机物可相互转化,故C正确;D.碳、氢、氧三种元素也参加了氮循环,如蛋白质的制造需要碳元素,又如N2在放电条件下与O2直接化合生成无色且不溶于水的一氧化氮气体,N2+O2![]() 2NO,氧元素参与,二氧化氮易与水反应生成硝酸(HN03)和一氧化氮,3NO2+H2O=2HNO3+NO,氢元素参加,故D正确;故答案为A;
2NO,氧元素参与,二氧化氮易与水反应生成硝酸(HN03)和一氧化氮,3NO2+H2O=2HNO3+NO,氢元素参加,故D正确;故答案为A;
(2)①一氧化氮易被氧气氧化为二氧化氮,2NO+O2=2NO2,二氧化氮可以和水之间反应生成硝酸和一氧化氮,即3NO2+H2O=2HNO3+NO,故答案为:3NO2+H2O=2HNO3+NO;
②在汽车尾气排放管中安装一个催化转化器,可将尾气中另一种有害气体CO跟NO反应转化为无毒气体二氧化碳和氮气,原理方程式为:2NO+2CO![]() N2+2CO2;
N2+2CO2;
③用NaOH吸收NO2和O2的混合气体生成NaNO3和水,根据电子守恒,发生反应的化学方程式是4NO2+O2+4NaOH=4NaNO3+2H2O;
(3)工业上利用NH3催化氧化生成NO、NO氧化为NO2,NO2溶于水得到HNO3,其中氨催化氧化生成NO的化学方程式为4NH3+5O2![]() 4NO+6H2O。
4NO+6H2O。


科目:高中化学 来源: 题型:
【题目】宏观物质的性质是由微观结构决定的。
(1)1998年,美国科学家合成了一种阳离子“NSn+”,其结构是对称的,5个N排成“V”形,如果5个N结合后都达到8电子结构,且含有2个N≡N。则n=__________,NSn+的电子式为______________________________。
(2)科学家们还获得了一种Na分子,分子中所有N原子均呈单键,且均满足8电子结构,试画出该分子的结构式__________________________。
(3)科学家们认为存在含氢量最高的化合物NH6,预测其与水剧烈反应入出气体,所得水溶液呈弱碱性。写出该反应的化学方程式__________,NH6的电子式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关合金的说法错误的是
A. 青铜是我国使用最早的合金 B. 钢是用量最大、用途最广的合金
C. 合金的硬度一般高于各成分金属 D. 合金的熔点一般高于各成分金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下图所示装置制取氨气。

(1)试管中发生反应的化学方程式是______________________________。
(2)干燥管中盛放的干燥剂是______________________________(填名称)。
(3)实验室中碳酸氢铵加热分解也可以制备氨气,该反应方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质之间进行反应时,可用离子方程式2H+ + CO32- → H2O+CO2 ↑表示的是
A. 碳酸钠溶液中加入足量醋酸溶液 B. 碳酸钡和稀硝酸反应
C. 碳酸氢钠溶液中加入少量稀硫酸 D. 在盐酸溶液中滴入少量碳酸钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,有0.01 molL-1的醋酸溶液,试回答下列问题:
(1)写出醋酸的电离平衡常数表达式_____________
(2)达平衡时,溶液中c(H+)=______________(25℃时,醋酸的K=1.75×10 -5)
(3)当向该溶液中加入一定量的盐酸时,溶液中的c(H+)_____,c (CH3COO-)_________(填增大、减小、不变)。
(4)当向该溶液中加入一定量的盐酸时,电离常数________ (填增大、减小、不变)。原因________________________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产生活密切相关。下列说法错误的是
A. 纤维素是多糖,可以作人类的营养物质
B. 利用高纯度单质硅可以制成太阳能光伏电池
C. 制作宇宙飞船的玻璃纤维和玻璃的成分相同
D. C1O2可用作自来水消毒剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知高铁酸钠(Na2FeO4)是一种绿色消毒净水剂,只在碱性环境中稳定存在。下列是通过次氧酸钠氧化法制备高铁酸钠并探究其性质的实验,步骤如下:
I.制备高铁酸钠(Na2FeO4)
(1)制备NaClO溶液
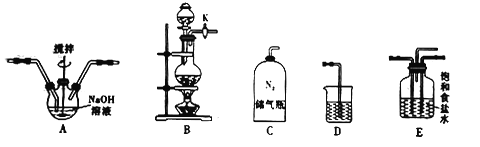
已知:3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O
5NaCl+NaClO3+3H2O
①如何检查装置B的气密性?____________________________________________。
②实验室制取Cl2的化学方程式是_______________________,利用如图所给的装置组装成制备NaClO的正确连接顺序是![]() ________(填字母),其中装置E的作用是________(填序号)。
________(填字母),其中装置E的作用是________(填序号)。
a.混合气体 b.除去氯气中的氯化氢 c.干燥气体 d.观察气体的通入速率
③为了防止产生NaClO3,除搅拌和混入N2稀释外,还应采取的操作是__________________。
(2)制备Na2FeO4:将Fe(NO3)2溶液加入到NaOH与NaClO的混合溶液中,其反应的离子方程式是___________________________________。
II.高铁酸钠(Na2FeO4)具有强氧化性,某实验小组的同学对于高铁酸钠消毒后铁元素的存在形式展开如下探究:
【提出猜想】:猜想1:全部为Fe2+ 猜想2:全部为Fe3+ 猜想3: Fe2+和Fe3+都有
【设计实验】:
(1)证明溶液中只含有Fe2+的实验操作是_________________________________。
(2)某实验小组将消毒后的溶液分在两支试管中,进行如下实验:
步骤一:向试管1中加入K3[Fe(CN)6]溶液,现象是__________,所以溶液中不存在Fe2+;
步骤二:向试管2中滴入KSCN溶液,溶液变成血红色,所以溶液中存在Fe3+。
【实验结论】:高铁酸钠消毒后溶液中只存在Fe3+。
(3)小明同学认为上述实验结论不够严谨,原因是___________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com