
【题目】某温度下,H2(g) + CO2(g) ![]() H2O(g)+ CO(g)的平衡常数K=9/4。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和 CO2(g),其起始浓度如下表所示
H2O(g)+ CO(g)的平衡常数K=9/4。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和 CO2(g),其起始浓度如下表所示
起始浓度 | 甲 | 乙 | 丙 |
C(H2)/ mol·l-1 | 0.010 | 0.020 | 0.020 |
C(CO2)/ mol·l-1 | 0.010 | 0.010 | 0.020 |
下列判断不正确的是
A. 平衡时,乙中CO2 的转化率大于60%
B. 平衡时,甲和丙中H2 的转化率均是60%
C. 平衡时,丙中C(CO2)是甲中的2倍,是0.012 mol·l-1
D. 反应开始时,丙中的反应速率最快,甲中的反应速率最慢
【答案】C
【解析】某温度下,H2(g) + CO2(g) ![]() H2O(g)+ CO(g)的平衡常数K=9/4。该反应是一个气体分子数不变的反应,所以压强不影响该反应的化学平衡状态。由甲的投料和该反应的平衡常数可以计算出,氢气和二氧化碳的平衡浓度都是0.004mol/L(设二氧化碳的变化量为x,则
H2O(g)+ CO(g)的平衡常数K=9/4。该反应是一个气体分子数不变的反应,所以压强不影响该反应的化学平衡状态。由甲的投料和该反应的平衡常数可以计算出,氢气和二氧化碳的平衡浓度都是0.004mol/L(设二氧化碳的变化量为x,则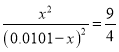 ,解之得x=0.006mol/L),氢气和二氧化碳的转化率均为
,解之得x=0.006mol/L),氢气和二氧化碳的转化率均为![]() 60%,丙和甲的投料的比例是相同的,所以丙和甲能建立等效平衡,丙和甲的反应物的转化率是相同的,但是它们的平衡浓度不同,丙中C(CO2)是甲中的2倍,是0.008 mol·l-1 。A. 平衡时,乙相当于在甲的平衡状态下再增大反应物氢气的浓度,化学平衡向正反应方向移动,所以乙中CO2 的转化率大于60%,A正确;B. 平衡时,甲和丙中H2 的转化率均是60%,B正确;C. 平衡时,丙中C(CO2)是甲中的2倍,是0.008 mol·l-1 ,C不正确;D. 反应开始时,丙中的反应物浓度最大,反应速率最快;甲中的反应物浓度最小,反应速率最慢,D正确。本题选C。
60%,丙和甲的投料的比例是相同的,所以丙和甲能建立等效平衡,丙和甲的反应物的转化率是相同的,但是它们的平衡浓度不同,丙中C(CO2)是甲中的2倍,是0.008 mol·l-1 。A. 平衡时,乙相当于在甲的平衡状态下再增大反应物氢气的浓度,化学平衡向正反应方向移动,所以乙中CO2 的转化率大于60%,A正确;B. 平衡时,甲和丙中H2 的转化率均是60%,B正确;C. 平衡时,丙中C(CO2)是甲中的2倍,是0.008 mol·l-1 ,C不正确;D. 反应开始时,丙中的反应物浓度最大,反应速率最快;甲中的反应物浓度最小,反应速率最慢,D正确。本题选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】镀锌铁在发生吸氧腐蚀时,若有0.2mol电子发生转移,下列说法正确的是( )
①有5.6g金属被腐蚀
②有6.5g金属被腐蚀
③在标准状况下有2.24L气体吸收
④在标准状况下有1.12L气体吸收.
A.①②
B.②③
C.①④
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中,两种气体的分子数一定相等的是( )
A. 温度相同、体积相同的O2和N2 B. 体积相等、密度不等的CO和C2H4
C. 质量相等、密度不等的N2和C2H4 D. 压强相同、体积相同的N2和O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从A.CaCO3 B.乙醇 C.次氯酸钠 三种物质中,选择合适的物质,将其标号填在横线上。
(1)“84消毒液”的成分是________; (2)常用作燃料和医用消毒剂的是________;
(3)烧水壶内壁附着的水垢成分之一是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】500mL KNO3和Cu(NO3)2的混合溶液中c(NO3﹣)=6.0mol/L,用铅蓄电池作电源,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,求(无相应计算过程不得分)
(1)原溶液中K+的浓度?
(2)铅蓄电池的正极质量改变多少?
(3)若将电解后的溶液恢复到电解前的浓度,加一种什么物质;其质量为多少克?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2A(g)+B(g)![]() 2C(g);ΔH =-a kJ/mol(a>0)。在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500℃时充分反应达平衡后C的浓度w mol/L,放出热量b kJ。
2C(g);ΔH =-a kJ/mol(a>0)。在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500℃时充分反应达平衡后C的浓度w mol/L,放出热量b kJ。
(1)比较a____b(填“>”“=”或“<”)。
(2)若在原来的容器中,只加入2 mol C,500℃ 时充分反应达到平衡后,吸收热量c kJ,C浓度__________w mol/L(填“>”“=”或“<”),a、b、c之间满足何种关系_______________(用a、b、c建立一个等式关系)。
(3)能说明该反应已经达到平衡状态的是____________(填写字母)。
A.v(C)=2v(B) B.容器内压强保持不变
C.v逆(A)=2v正(B) D.容器内的密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的操作是_______(填写字母)。
A.及时分离出C气体 B.适当升高温度
C.增大B的浓度 D.选择高效的催化剂
(5)若将上述容器改为恒压容器(反应前体积、压强相同),起始时加入2 mol A和1 mol B,500℃时充分反应达平衡后,放出热量d kJ ,则d________b(填“>”、“=”或“<”),理由是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com