
某校化学小组学生利用下图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3·6H2O晶体。(图中夹持及尾气处理装置均已略去)
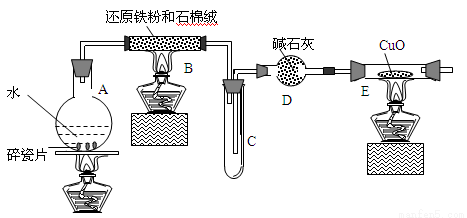
(1)装置B中发生反应的化学方程式是 。
(2)装置E中的现象是 。
(3)停止反应,待B管冷却后,取其中的固体,加入过量稀盐酸充分反应,过滤。简述检验滤液中Fe3+的操作方法:
(4)该小组利用上述滤液制取FeCl3·6H2O晶体,设计流程如下:滤液(步骤I)→FeCl3溶液(步骤II)→FeCl3·6H2O晶体
①步骤I中通入Cl2的作用是 。
②步骤II从FeCl3稀溶液中得到FeCl3·6H2O晶体的主要操作包括: 。③该流程中需保持盐酸过量,主要原因是(结合离子方程式简要说明)________________
(1)3Fe+4H2O(g) Fe3O4+4H2 (3分)
Fe3O4+4H2 (3分)
(2)黑色固体变为红色,管壁有水珠(2分)
(3)取少量滤液,滴入几滴KSCN溶液,观察溶液是否变红色(2分)
(4)①将滤液中含有的Fe2+氧化成Fe3+(3分)
②蒸发浓缩、冷却结晶、过滤(3分)
③FeCl3会发生水解反应,即3Fe3++3H2O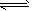 Fe(OH)3+3H+,过量盐酸能抑制FeCl3的水解(3分)
Fe(OH)3+3H+,过量盐酸能抑制FeCl3的水解(3分)
【解析】
试题分析:(1)装置B中铁粉与水蒸气在高温下发生反应生成四氧化三铁和氢气,反应的化学方程式为:3Fe+4H2O(g) Fe3O4+4H2;(2)装置B铁与水蒸气反应生成的氢气,经碱石灰干燥后进入装置E,氧化铜与氢气加热发生反应生成了铜和水,所以反应的现象为:黑色的粉末变成红色,管壁产生水珠;(3)检验Fe3+离子的方法为:取少量滤液,滴入几滴硫氰化钾溶液,观察溶液是否变红色;(4)①步骤I中通入Cl2的作用是将Fe2+氧化成Fe3+,且产生FeCl3而不会引入杂质;②步骤II从FeCl3稀溶液中得到FeCl3·6H2O晶体,为防止水解,应有氯化氢气体的氛围中蒸发浓缩、冷却结晶、过滤,才能得到FeCl3·6H2O晶体;③由于水解产生的盐酸易挥发,故该流程中需保持盐酸过量或在氯化氢氛围中加热蒸发,否则会发生水解反应:3Fe3++3H2O
Fe3O4+4H2;(2)装置B铁与水蒸气反应生成的氢气,经碱石灰干燥后进入装置E,氧化铜与氢气加热发生反应生成了铜和水,所以反应的现象为:黑色的粉末变成红色,管壁产生水珠;(3)检验Fe3+离子的方法为:取少量滤液,滴入几滴硫氰化钾溶液,观察溶液是否变红色;(4)①步骤I中通入Cl2的作用是将Fe2+氧化成Fe3+,且产生FeCl3而不会引入杂质;②步骤II从FeCl3稀溶液中得到FeCl3·6H2O晶体,为防止水解,应有氯化氢气体的氛围中蒸发浓缩、冷却结晶、过滤,才能得到FeCl3·6H2O晶体;③由于水解产生的盐酸易挥发,故该流程中需保持盐酸过量或在氯化氢氛围中加热蒸发,否则会发生水解反应:3Fe3++3H2O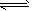 Fe(OH)3+3H+,利用过量盐酸能抑制FeCl3的水解。
Fe(OH)3+3H+,利用过量盐酸能抑制FeCl3的水解。
考点:考查铁及其化合物的性质实验。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届广东省海珠等四区高三联考理综化学试卷(解析版) 题型:填空题
(16分)已知合成氨的反应为3H2(g)+N2(g) 2NH3(g) △H<0,在某密闭容器中测得实验数据及数据处理如下表。
2NH3(g) △H<0,在某密闭容器中测得实验数据及数据处理如下表。
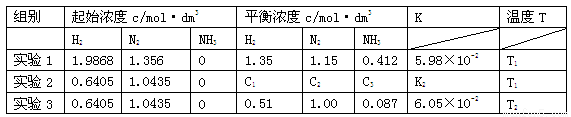
(1)下列说法可以说明合成氨反应达到平衡的是
A.恒容时,整个容器内密度不变
B.恒压时,容器内平均相对分子质量不变
C.1 mol N≡N键断裂的同时,有3mol H-H键断裂
(2)当升高温度时,平衡向 方向移动(填“正”或“逆”),请画出在t2时刻升温后的v-t图,并作出必要的标注。

(3)表中实验2的K2= ,温度T1、T2的大小关系是 ,你判断的理由是 。
查看答案和解析>>
科目:高中化学 来源:2015届广东省广州市高三9月第二次月考化学试卷(解析版) 题型:选择题
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是
| X | Y | Z |
① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
② | KOH溶液 | SiO2 | 稀盐酸 |
③ | O2 | N2 | H2 |
④ | FeCl3溶液 | Cu | 浓硝酸 |
A.①③ B.①④ C.②④ D.②③
查看答案和解析>>
科目:高中化学 来源:2015届广东省增城市毕业班调研测试理科综合化学试卷(解析版) 题型:实验题
(16分)白钨矿的主要成分是CaWO4 ,含有二氧化硅、氧化铁等杂质,工业生产钨流程如下:

(完全沉淀离子的pH值:SiO32-为8,WO42-为5)
(1)白钨矿反应前需要进行粉碎,其目的是____________。CaWO4与纯碱发生的化学反应方程式是_______________________________。
(2)滤渣A的主要成分是(写化学式)_____________,滤渣B的化学式是__________。
(3)调节pH可选用的试剂是:__________。
A.氨水 B.氢氧化钠溶液 C.盐酸
(4)母液中加入盐酸的离子方程式为________________________________________。
(5)白钨矿中CaWO4的质量分数为30%,576千克白钨矿理论上最多能生产钨_____kg。(已知钨酸钙的相对分子质量为288)
查看答案和解析>>
科目:高中化学 来源:2015届广东省增城市毕业班调研测试理科综合化学试卷(解析版) 题型:选择题
设nA为阿伏加德罗常数的数值,下列说法正确的是
A.常温常压下,16 g O2含有nA个氧原子
B.1mol苯含有3nA个碳碳单键和3nA个碳碳双键
C.一定条件下,3molH2和1molN2充分反应后,可得到2nA个NH3分子数
D.1 mol·L-1 FeCl3溶液中含有Cl-总数为3nA
查看答案和解析>>
科目:高中化学 来源:2015届广东省佛山市高三10月月考化学试卷(解析版) 题型:选择题
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图。
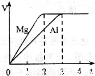
反应中镁和铝的
A.物质的量之比为3:2 B.质量之比为3:2
C.摩尔质量之比为2:3 D.反应速率之比为2:3
查看答案和解析>>
科目:高中化学 来源:2015届广东省佛山市高三9月考化学试卷(解析版) 题型:填空题
(11分)以食盐为原料进行生产并综合利用的某些过程如下图所示。
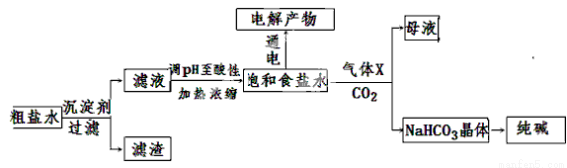
(1)除去粗盐中的Ca2+、Mg2+和SO42-离子,加入下列沉淀剂的顺序是(填字母) 。
a.Na2CO3 b.NaOH c.BaCl2
(2)将滤液的pH调至酸性除去的离子是 。
(3)电解饱和食盐水可得到H2和另外两种产物,这两种物质相互反应的离子方程式为 ,欲从饱和食盐水中获得食盐晶体,可采用的实验方法是 。
(4)气体X可增大饱和食盐水吸收CO2的量,有利于NaHCO3晶体的生成和析出,X的化学式是 。
(5)下列有关NaHCO3和纯碱的说法正确的是 (填字母)
A.NaHCO3属于盐类,纯碱属于碱
B.分别往同浓度的NaHCO3溶液和纯碱溶液中滴加稀盐酸,产生气泡的速率相同
C.常温下在水中的溶解度,NaHCO3大于纯碱
D.除去NaHCO3溶液中的纯碱,应往溶液中通入足量的CO2
查看答案和解析>>
科目:高中化学 来源:2015届广东省佛山市高三9月考化学试卷(解析版) 题型:选择题
下列离子在指定条件下能大量共存的是
A.在酸性溶液中:Ba2+、K+、SO32―、Cl―
B.含有大量Al3+的溶液中:K+、Na+、NH4+、SO42―
C.使甲基橙变黄的溶液中:Na+、I―、CO32―、OH―
D.无色溶液中:K+、Cl―、Cr2O72-、HCO3―
查看答案和解析>>
科目:高中化学 来源:2015届广东省中山市等五校联考高三第一学期化学试卷(解析版) 题型:选择题
相同质量的铜片分别与过量的体积相同的浓硝酸、稀硝酸反应,二者相比较,相等的是
A.铜片完全消耗时所用的时间
B.反应中转移的电子总数
C.反应所消耗硝酸的物质的量
D.反应生成气体的体积(标准状况)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com