
 .水源中的NO3-对人类健康会产生危害.为了降低水源中NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为10Al+6NO3-+4OH-=10AlO2-+3N2↑+2H2O,此方法的缺点是处理后的水中生成了A1O3-,仍然可能对人类健康产生危害,还需要对该饮用水进行一系列后续处理.
.水源中的NO3-对人类健康会产生危害.为了降低水源中NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为10Al+6NO3-+4OH-=10AlO2-+3N2↑+2H2O,此方法的缺点是处理后的水中生成了A1O3-,仍然可能对人类健康产生危害,还需要对该饮用水进行一系列后续处理.分析 (1)铝的化学性质比较活泼,而铝在空气中稳定存在,是因表面生成致密的氧化膜;
(2)氟化铵水解生成氢氟酸,氢氟酸能够与玻璃中二氧化硅反应;
(3)A、氢氧化铝可以治疗胃酸过多;
B、耐火材料应具有较高的熔点;
C、铝热剂为铝和金属氧化物;
D、氧化铝属于两性氧化物,可以和强酸反应又能和强碱反应;
(4)NOCl分子中各原子均满足8电子稳定结构,则氮原子与氧原子形成两对共用电子对,与氯原子形成一对;根据题干信息,反应物为:铝、NO3-、OH-,生成物为:N2、H2O、碱性条件下铝参加反应生成物还有AlO2-,根据电子守恒和原子守恒书写方程式;
依据Al(OH)3?AlO2-+H++H2O K=1.0×10-13,结合水中AlO2-浓度降到1.0×10-6mol•L-1,计算氢离子浓度;依据Ksp[Al(OH)3]=1.3×10-33,计算铝离子浓度.
解答 解:(1)铝在空气中稳定存在,其原因是在常温下Al与氧气反应,铝表面能形成致密的氧化膜,能保护内层金属不被氧化,反应的化学方程式为4Al+3O2=2Al2O3,
故答案为:4Al+3O2=2Al2O3,铝表面能形成致密的氧化膜,能保护内层金属不被氧化;
(2)氟化铵中的氟离子水解生成氢氟酸,氢氟酸能够与玻璃中二氧化硅反应,对玻璃有强烈的腐蚀性而对塑料则无腐蚀性,所以该实验所用试管及盛装NH4F溶液的试剂瓶均为塑料材质;
故答案为:氟化铵中的氟离子水解生成氢氟酸,氢氟酸能够与玻璃中二氧化硅反应,对玻璃有强烈的腐蚀性而对塑料则无腐蚀性;
(3)A、氢氧化铝可以治疗胃酸过多,氧化铝不可以,故A错误;
B、氧化铝熔点高,可以作优良的耐火材料,故B正确;
C、铝热剂为铝和其他金属氧化物,则铝是铝热剂的成分之一,不是氧化铝,故C错误;
D、氧化铝属于两性氧化物,可以和强酸反应又能和强碱反应,不能与弱碱氨水反应,故D错误;
故选:B;
(4)NOCl分子中各原子均满足8电子稳定结构,则氮原子与氧原子形成两对共用电子对,与氯原子形成一对,电子式为 ;
;
根据题干信息,反应物为:铝、NO3-、OH-,生成物为:N2、H2O、碱性条件下铝参加反应生成物还有AlO2-,反应中Al→AlO2-,Al元素化合价由0价升高为+3价,共升高3价,NO3-→N2↑,氮元素化合价由+5价降低为0价,共降低10价,化合价升降最小公倍数为30,依据原子个数守恒、电荷守恒反应的离子方程式:10Al+6NO3-+4OH-=10AlO2-+3N2↑+2H2O;水中AlO2-浓度降到1.0×10-6mol•L-1,依据Al(OH)3?AlO2-+H++H2O K=1.0×10-13,则C(H+)=$\frac{1.0×10{\;}^{-13}}{1.0×10{\;}^{-6}}$=10-7(mol/L);pH=7,C(OH-)=10-7mol/L,:25℃时,Ksp[Al(OH)3]=1.3×10-33,则C(Al3+)=$\frac{1.3×10{\;}^{-33}}{(10{\;}^{-7}){\;}^{3}}$=1.3×10-12mol•L-1;
故答案为: ;10Al+6NO3-+4OH-=10AlO2-+3N2↑+2H2O;7;1.3×10-12mol•L-1.
;10Al+6NO3-+4OH-=10AlO2-+3N2↑+2H2O;7;1.3×10-12mol•L-1.
点评 本题为综合题,考查了金属的防腐、离子方程式、方程式的书写等,熟悉铝及其化合物性质是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
 X、Y、Z为原子序数依次增大的短周期主族元素,三种元素属于不同周期.下列转化关系中,A、B、C是X、Y、Z对应的三种气态单质,其余均为常见化合物.下列分析正确的是( )
X、Y、Z为原子序数依次增大的短周期主族元素,三种元素属于不同周期.下列转化关系中,A、B、C是X、Y、Z对应的三种气态单质,其余均为常见化合物.下列分析正确的是( )| A. | 离子半径:Y>Z | B. | Z的含氧酸均有强氧化性 | ||
| C. | 与Y同周期氢化物中D最稳定 | D. | F含离子键和共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 室温时,将0.10mol/L NaOH溶液滴入20.00mL未知浓度的某一元酸HA溶液中,溶液pH随加入NaOH溶液体积的变化曲线如图.当V(NaOH)=20.00mL,二者恰好完全反应.则下列有关说法不正确的是( )
室温时,将0.10mol/L NaOH溶液滴入20.00mL未知浓度的某一元酸HA溶液中,溶液pH随加入NaOH溶液体积的变化曲线如图.当V(NaOH)=20.00mL,二者恰好完全反应.则下列有关说法不正确的是( )| A. | 该一元酸溶液浓度为0.10 mol•L-1 | |
| B. | a、b、c点的水溶液导电性依次增强 | |
| C. | 室温时,HA的电离常数Ka≈l×10-5 | |
| D. | a点和c点所示溶液中H2O的电离程度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题

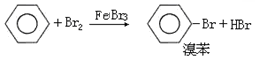 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某学习小组拟研究化学平衡建立以及浓度对化学平衡移动的影响.
某学习小组拟研究化学平衡建立以及浓度对化学平衡移动的影响.| 实验编号 | ① | ② | ③ | |
| 加入试剂 | 5mL 6mol/L FeCl3溶液和5滴0.03mol/L 的KSCN溶液 | 少量铁粉 | 5mL水 | 5mL NaOH溶液 |
| 现象预期 | 红色加深 | 溶液红色变浅 | 加入5mL NaOH溶液后,溶液颜色较加5mL水后更浅(填“更深”“更浅”或“相同”) | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
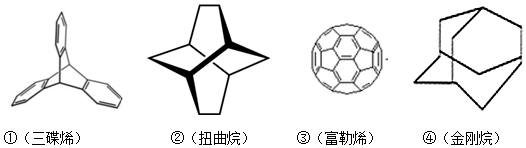
| A. | ①③均能发生加成反应 | B. | ①④互为同分异构体 | ||
| C. | ①②③④均属于烃 | D. | ①②③④的一氯代物均只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等质量的CO、N2含有的分子数均为NA | |
| B. | 0.5 mol/L的MgCl2溶液中Cl-离子的物质的量为NA | |
| C. | 常温常压时,4.48 L CH4气体中含有的原子数大于NA | |
| D. | 12克13C含有的碳原子数小于NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com