
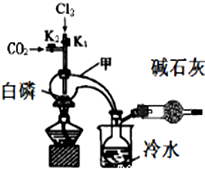
 三氯化磷(PCl3)是合成药物的重要化工原料,可通过白磷和氯气化合得到.
三氯化磷(PCl3)是合成药物的重要化工原料,可通过白磷和氯气化合得到.| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 |
| 白磷 | 44.1 | 280.5 | 1.82 |
| PCl3 | -112 | 75.5 | 1.574 |
| POCl3 | 2 | 105.3 | 1.675 |
分析 (1)实验室制取氯气用浓盐酸与MnO2 在加热的条件下进行,装置采用固体和液体加热制取气体的装置,所以实验过程中所用的玻璃仪器除酒精灯和玻璃导气管外,还需要的玻璃仪器有圆底烧瓶和分液漏斗;水和硫酸铜反应生成蓝色的硫酸铜,可以使用硫酸铜粉末检验干燥的氯气没有漂白性,潮湿的氯气具有漂白性,可以使用干燥有色布条褪色检验;
(2)PCl3遇O2会生成POCl3(三氯氧磷),所以向通入CO2 将空气赶走,白磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5,然后在加入白磷,氯气最后通,白磷熔沸点低,最后加热;
(3)PCl3 的沸点较低,E烧杯中加入冷水的目的是冷却收集PCl3,POCl3和PCl3遇水会强烈水解,干燥管中碱石灰的作用是吸收多余的氯气和空气中的水蒸气;
(4)根据表格提供的信息,物质互溶且熔沸点不同,除去PCl3中的POCl3选用的方法是蒸馏法;
(5)①PCl3遇水会强烈水解生成H3PO3和HCl,亚磷酸(H3PO3)是二元弱酸,分别电离,一步比一步艰难,而HCl是强酸,全部电离;
②若将0.01 mol POCl3投入热水配成1 L的溶液,发生的化学反应为POCl3+H2O=H3PO4+3HCl,盐酸是强酸,Cl-浓度为0.03mol/L,H3PO4 是中强酸,分步电离,以第一步电离为主,产生的PO43-的浓度很小,结合溶度积,逐滴加入AgNO3溶液,则先产生的沉淀是AgCl.
解答 解:(1)实验室制取氯气用浓盐酸与MnO2 在加热的条件下进行,装置采用固体和液体加热制取气体的装置,所以实验过程中所用的玻璃仪器除酒精灯和玻璃导气管外,还需要的玻璃仪器有:圆底烧瓶和分液漏斗;水和硫酸铜反应生成蓝色的硫酸铜,干燥的氯气没有漂白性,所以证明通入的氯气是干燥的方法是:将气体通过装有无水硫酸铜的U形管(干燥管),若白色粉末未变蓝,则气体干燥,或者将氯气通入装有干燥的有色布条的集气瓶,布条不褪色,说明氯气是干燥的,
故答案为:圆底烧瓶、分液漏斗;将气体通过装有无水硫酸铜的U形管(干燥管),若白色粉末未变蓝,则气体干燥(或者通入装有干燥的有色布条的集气瓶,布条不褪色等,或者将氯气通入装有干燥的有色布条的集气瓶,布条不褪色,说明氯气是干燥的,合理答案均可);
(2)PCl3遇O2会生成POCl3(三氯氧磷),所以向通入CO2 将空气赶走,白磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5,然后在加入白磷,氯气最后通,白磷熔沸点低,最后加热,具体操作为:在甲中先加入白磷,再通入CO2到排尽甲中的空气,向甲中通入Cl2,加热,
故答案为:在甲中先加入白磷,再通入CO2到排尽甲中的空气,向甲中通入Cl2,加热;
(3)PCl3 的沸点较低,所以E烧杯中加入冷水的目的是冷却收集PCl3,POCl3和PCl3遇水会强烈水解,干燥管中碱石灰的作用是吸收多余的氯气和空气中的水蒸气,
故答案为:冷却PCl3,使其液化;吸收多余的氯气和空气中的水蒸气;
(4)根据表格提供的信息,它们互溶且熔沸点不同,所以除去PCl3中的POCl3制备纯净的PCl3可选用的方法是蒸馏法,
故选:C;
(5)①PCl3遇水会强烈水解生成H3PO3和HCl,亚磷酸(H3PO3)是二元弱酸,分别电离,一步比一步艰难,而HCl是强酸,全部电离,溶液中离子浓度顺序为:c(H+)>c(Cl-)>c(H2PO3-)>c(HPO32-),
故答案为:c(H+)>c(Cl-)>c(H2PO3-)>c(HPO32-);
②若将0.01 mol POCl3投入热水配成1 L的溶液,发生的化学反应为POCl3+H2O=H3PO4+3HCl,盐酸是强酸,Cl-浓度为0.03mol/L,H3PO4 是中强酸,分步电离,以第一步电离为主,产生的PO43-的浓度很小,根据Ksp(Ag3PO4)=1.4×10-16,Ksp(AgCl)=1.8×10-10,逐滴加入AgNO3溶液,则先产生的沉淀是AgCl,
故答案为:AgCl.
点评 本题考查氯气的实验室制法、PCl3的制备、离子浓度的大小比较、沉淀溶解平衡等知识,是对学生综合能力的考查,需要学生具备扎实的基础与灵活运用能力,难度中等.


 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案科目:高中化学 来源: 题型:推断题
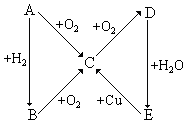 根据如图所示的A、B、C、D、E五种物质的相互转化关系,按如下要求填写相应的物质和有关反应的化学方程式.
根据如图所示的A、B、C、D、E五种物质的相互转化关系,按如下要求填写相应的物质和有关反应的化学方程式.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
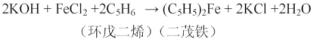
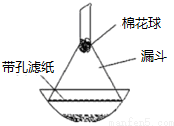
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
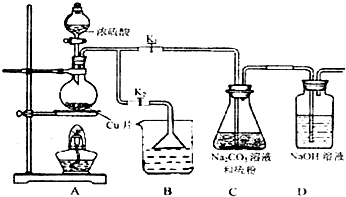
| 编号 | 1 | 2 | 3 | 4 |
| 消耗Na2S2O3标准溶液的体积/mL | 18.02 | 17.98 | 18.00 | 20.03 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
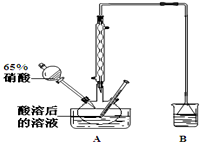 亚硝酸钠可大量用于染料和有机合成工业.
亚硝酸钠可大量用于染料和有机合成工业.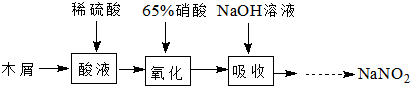
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
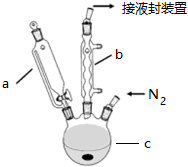
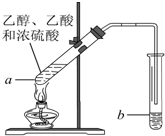 在实验室可以在试管a中加入3mL 乙醇,然后边振荡试管边慢慢加入2mL浓硫酸和2mL 乙酸,按下图所示,连接好装置进行实验,以制取乙酸乙酯.回答下列问题:
在实验室可以在试管a中加入3mL 乙醇,然后边振荡试管边慢慢加入2mL浓硫酸和2mL 乙酸,按下图所示,连接好装置进行实验,以制取乙酸乙酯.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化 学 键 | H-H | I-I |
| 断开1mol化学键时吸收的能量(kJ) | b | c |
| A. | 该反应中反应物的总能量高于生成物的总能量 | |
| B. | 断开1 mol H-H 键和1 mol I-I 键所需能量大于断开2 mol H-I 键所需能量 | |
| C. | 断开2 mol H-I键所需能量为(a+b+c)kJ | |
| D. | 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com