
(��10��) �״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ������ҵ��һ������������ַ�Ӧ�ϳɼ״�����Ӧ��CO(g)+2H2(g)  CH3OH(g)����H1
CH3OH(g)����H1
��Ӧ��C02(g)+3H2(g)  CH30H(g)+ H2O(g)����H2
CH30H(g)+ H2O(g)����H2
�±����������Ƿ�ӦI�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ��(K)��
�¶� | 250�� | 300�� | 350�� |
K | 2.O | 0.27 | 0.012 |
��1����һ�������½�2 molCO��6molH2����2L���ܱ������з�����ӦI��5min����c(CO)=0.4 mol��L������˶�ʱ��ķ�Ӧ����(��H2��ʾ) mol��(L��min)��
��2���ɱ��������жϡ�H1 0(�>������<����=��)��ӦC02(g)+H2(g) CO(g)+H20(g)��H3= (�á�H1�͡�H2��ʾ)��
CO(g)+H20(g)��H3= (�á�H1�͡�H2��ʾ)��
��3���������ݻ����䣬���д�ʩ����߷�Ӧ����COת���ʵ��� (ѡ��ĸ)��
a������CO��ʹ��ϵ��ѹǿ����
b����CH3OH(g)����ϵ�з���
e������He��ʹ��ϵ��ѹǿ����
d��ʹ�ø�Ч����
��4��д����Ӧ��Ļ�ѧƽ�ⳣ������ʽ��K= �����ֺ��º��ݵ������½���Ӧ���ƽ����ϵ������Ũ�Ⱦ�����һ������ѧƽ�� (�������������)�ƶ���ƽ�ⳣ��K (��������С�����䡱)��
��5�������ֺϳɼ״��ķ����Ƚϣ�ԭ�������ʽϸߵ��� (���)��
21.��1�� 0.24 ��2�� �� , ��H2 - ��H1 ��3�� b
��4�� C��CH3 OH��C��H2 O��/ C��C O2��C3��H2��, ���� ������ ��5�� ��
��������
�����������1��COŨ�ȱ仯��Ϊ2/2mol/L -0.4mol/L=0.6mol/L��v��CO��=0.6/5=0.12mol/��L?min��������֮�ȵ��ڻ�ѧ������֮�ȣ�=v��H2��=2v��CO��=2��0.12mol/��L?min��=0.24mol/��L?min��;
��2���ɱ������ݿ�֪�����¶����ߣ�ƽ�ⳣ��K��С��˵���¶����ߣ�ƽ��������У����������Ƿ��ȷ�Ӧ������H1 < 0�����ݸ�˹���ɣ�C02(g)+H2(g)  CO(g)+H20(g)��H3=��H2 - ��H1��
CO(g)+H20(g)��H3=��H2 - ��H1��
��3��a������CO��ʹ��ϵ��ѹǿ����ƽ��������Ӧ�ƶ�����CO��ת���ʽ��ͣ�a����b����CH3OH��g������ϵ�з��룬ƽ��������Ӧ�����ƶ���COת��������b��ȷ��c������He��ʹ��ϵ��ѹǿ�������ʵ�Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���COת���ʲ��䣬c����d��ʹ�ø�Ч���������ܸı�ƽ�⣬d����ѡb����4����4����Ӧ��CO2��g��+3H2��g��?CH3OH��g��+H2O��g����ƽ�ⳣ��k=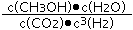 �����ֺ��º��ݵ������½���Ӧ���ƽ����ϵ������Ũ�Ⱦ�����һ�������ݵ�Чƽ�����ۣ��൱������ѹǿ����ѧƽ�������ƶ�����Ϊ�¶Ȳ��䣬ƽ�ⳣ��KҲ���䣻��5�������ֺϳɼ״��ķ����Ƚϣ�ԭ�������ʽϸߵ��Ǣ�Ϊ100%����
�����ֺ��º��ݵ������½���Ӧ���ƽ����ϵ������Ũ�Ⱦ�����һ�������ݵ�Чƽ�����ۣ��൱������ѹǿ����ѧƽ�������ƶ�����Ϊ�¶Ȳ��䣬ƽ�ⳣ��KҲ���䣻��5�������ֺϳɼ״��ķ����Ƚϣ�ԭ�������ʽϸߵ��Ǣ�Ϊ100%����
���㣺���黯ѧ��Ӧ���ʵļ��㣬��ѧƽ�ⳣ����Ӱ��ƽ������أ�ƽ��ת���ʵ�֪ʶ��


 ������ȫ�̼����ĩ���100��ϵ�д�
������ȫ�̼����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ӱ�ʡ�����и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
д��1---18��Ԫ���з�������������ԭ�ӣ����ӣ��ṹʾ��ͼ��
��ԭ�Ӻ���M���Ӳ�����2�����ӵ�ԭ�ӣ�
�ڵõ�2�����Ӻ�����Ӳ�ṹ��Ne��ͬ�����ӣ�
��������һ����λ������ɣ��˵����Ϊ11��
����������18�����ӣ���ʧȥ1������ʱ�ʵ����ԣ�
���������磬��������Ϊ1
����д�������Ľṹʾ��ͼ �� ��
�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ�����и�һ��ѧ�ڵ�һ���¿���ѧ���������棩 ���ͣ�ѡ����
��NA��ʾ�����ӵ�������ֵ������������ȷ����( )
A������NA����ԭ�ӵĺ����ڱ�״���µ����ԼΪ11��2 L
B��25�棬1��01��105 Pa��64 g SO2�к��е�ԭ����Ϊ3NA
C���ڳ��³�ѹ�£�11��2 L Cl2���еķ�����Ϊ0��5 NA
D����״���£�11��2 L�Ҵ����еķ�����Ϊ0��5 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ�������һ��ѧ�����л�ѧ�������Ծ��������棩 ���ͣ�ѡ����
24 mL0.05 mol��L-1��Na2SO3��Һǡ����40 mL 0.02 mol��L-1��K2RO4������Һ��Ӧ���������ƣ���Ԫ��R�ڻ�ԭ�����еļ�̬��
A��+6 B����3 C����2 D��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ�������һ��ѧ�����л�ѧ�������Ծ��������棩 ���ͣ�ѡ����
���³�ѹ�£��õ�������CH4��CO2��O2��SO2��������ֱ��ĸ�������������ΪCH4����
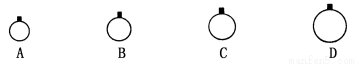
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ�������и߶���ѧ�����л�ѧ�������Ծ��������棩 ���ͣ�ѡ����
��ij�ݻ�һ�����ܱ������У������еĿ��淴Ӧ��A��g��+B��g�� xC��g������ͼ����ʾ�ķ�Ӧ���ߣ����ж϶�ͼ���˵����ȷ���ǣ�T��ʾ�¶ȣ�P��ʾѹǿ��C%��ʾC�����������
xC��g������ͼ����ʾ�ķ�Ӧ���ߣ����ж϶�ͼ���˵����ȷ���ǣ�T��ʾ�¶ȣ�P��ʾѹǿ��C%��ʾC�����������
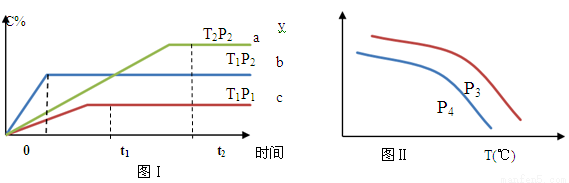
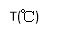
A.P3��P4��y���ʾB���������
B.P3��P4��y���ʾB��ת����
C.P3��P4��y���ʾ���������ܶ�
D.P3��P4��y���ʾ��������ƽ��Ħ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ�������и߶���ѧ�����л�ѧ�������Ծ��������棩 ���ͣ�ѡ����
�е��������pHֵ��Ba(OH)2��NaOH��NH3��H2O���ּ���Һ���μӵ�Ũ�ȵ����Ὣ����ǡ���кͣ���ȥ�������ֱ�ΪV1��V2��V3�������ߵĴ�С��ϵ��ȷ����
A.V3>V2>V1 C.B.V3=V2=V1 C.V3>V2=V1 C.D.V1=V2>V3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ������ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��50 mLijδ֪Ũ�ȵ�AlCl3��Һ�ֱ�ӵ�60 mL 1 mol��L��1��NaOH��Һ��60 mL 3 mol��L��1��NaOH��Һ�У����ܵõ�1��56 g Al(OH)3���������AlCl3��Һ��Ũ�ȿ����ǣ� ��
A��1 mol��L��1 B��0��5 mol��L��1 C��0��6 mol��L��1 D��0��4 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭�����Ƹ۶����صڶ���ѧ��һ�ϵ�һ���¿���ѧ���������棩 ���ͣ�ѡ����
�ڱ�״���£���ռ���������( )
A��98 g H2SO4 B��6.02��1023��N2���� C��44.8 L HCl D��6 g H2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com