
 Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放出的热量使部分H2O2受热分解:2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:
Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放出的热量使部分H2O2受热分解:2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,今做如下实验:分析 (1)用量筒量取液体时应选择体积接近的量筒,以减少误差;
(2)酸性和强氧化性的物质应选择酸式滴定管;
(3)排水法侧气体体积时,量筒内的液面要和水槽中液面相平,所得结果是常温常压下的气体体积;
(4)高锰酸钾具有氧化性,双氧水具有还原性,二者可以发生氧化还反应,高锰酸钾具有紫色;
(5)过氧化钠的纯度=$\frac{过氧化钠质量}{混合物质量}$×100%.
解答 解:(1)用量筒时应选择体积接近的量筒,以减少误差,所以收集112mL气体应选择150mL的量筒,
故答案为:150mL;
(2)高锰酸钾是强氧化性的物质,应选择酸式滴定管,
故答案为:酸式;
(3)在步骤③测量气体体积时,必须待烧瓶和量筒内的气体都冷却到室温时进行,此时量筒内的液面高于水槽中液面,立即读数会使收集到的气体体积偏高,结果偏高,应慢慢把量筒往下移,使量筒中液面恰好与水槽中液面相平,
故答案为:偏高;应慢慢把量筒往下移,使量筒中液面恰好与水槽中液面相平;
(4)高锰酸钾具有氧化性,双氧水具有还原性,二者可以发生氧化还反应,即2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O,高锰酸钾具有紫色,不需要指示剂来判断滴定终点,当溶液刚好出现浅紫红色,并在半分钟内不褪色,表明达到滴定终点,
故答案为:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O;滴入最后一滴溶液刚好由无色变为浅紫红色,且在半分钟内不褪色;
(5)双氧水分解掉的量,据2H2O2═2H2O+O2↑,当生成112mL氧气时,分解掉双氧水$\frac{0.112}{22.4}$×2=0.01(mol),
根据反应2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O求的剩余双氧水的量$\frac{5×24.2×0.01×1{0}^{-3}×10}{2.0g}$≈0.00605mol,所以双氧水的总量=0.01mol+0.00605mol=0.01605mol,根据反应Na2O2+2H2O═2NaOH+H2O2,可知过氧化钠的量为0.001605mol,纯度=$\frac{0.001605mol×78g/mol}{2.0g}$×=62.6%,
故答案为:62.6%.
点评 本题是一道定量计算题,主要是实验测定方法和实验步骤的理解应用,考查学生分析和解决问题的能力,综合性较强,难度很大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| 阳离子 | Na+、Al3+、Ba2+、NH4+ |
| 阴离子 | Cl-、OH-、CO32-、SO42- |
 ,B所含的阳离子是Ba2+.
,B所含的阳离子是Ba2+.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | T℃时,KW=1.0×10-12.该温度下,PH=3的溶液中,水电离出的c(H+)=1.0×10-11 | |
| B. | 25℃时,PH=a的氨水与PH=b的盐酸等体积混合至溶液呈中性,则a+b=14 | |
| C. | 0.1mol/LNaHCO3溶液中:c(HCO3-)>c(CO32-)>c(H2CO3) | |
| D. | 0.1mol/LCH3COOH溶液与0.05mol/LNaOH溶液等体积混合,所得溶液中,2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向FeSO4溶液中加入少量Na2O2:4Na2O2+6H2O+4Fe2+═4Fe(OH)3↓+8Na++O2↑ | |
| B. | 向明矾溶液中逐滴加入Ba(OH)2溶液至沉淀的质量最大:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| C. | 向NaClO溶液中通入少量SO2: 2ClO-+SO2+H2O═2HClO+SO32- | |
| D. | 将0.2 mol/L的NH4Al(SO4)2溶液与0.4 mol/L的Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-═Al(OH)3↓+2BaSO4↓+NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ′
′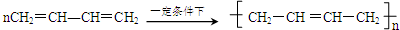 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阴离子 | CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com