
(1)下列有关实验操作或判断正确的是 (填序号,多选扣分)。
A.将配制好一定物质的量浓度的溶液,注入含有少量水的试剂瓶中,浓度不受影响。
B.用托盘天平称取5.85g氯化钠固体
C.苯、CCl4可用来萃取溴水中的溴。
D.需要95 mL 0.1 mol/L NaCl溶液,一般用100 mL容量瓶进行配制。
E.在天平左右两盘中各放一张白纸后,即可将NaOH固体放在白纸上称量。
F.观察钾元素焰色反应的操作是:先将铂丝放在稀盐酸中洗涤,然后蘸取固体氯化钾,置于酒精灯的火焰上进行灼烧,观察观察火焰的颜色。
(2)①容量瓶上含有下列量中的(填写字母)
A 压强 B 温度 C 容积 D 密度 E 刻度线
②用浓硫酸配制500mL2mol?L-1硫酸溶液时,所需的玻璃仪器除烧杯、量筒、玻璃棒和胶头滴管之外,还需要 (填仪器名称);在下列配制过程示意图中,有错误的是 (填写序号。
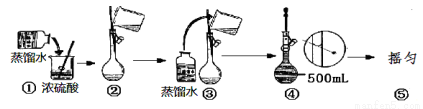
③现要用容量瓶配制500mL0.4mol?L-1Na2CO3溶液,配好的溶液倒入试剂瓶后需要贴上标签。请你帮助把下图标签上的内容填上去。

④下列情况将使配制溶液的物质的量浓度偏低的有 (填序号)。
A. 容量瓶用蒸馏水洗净后,未待干燥便用来配制
B. NaOH溶解后趁热移入容量瓶中
C. 定容时,俯视刻度线
D. 摇匀后发现液面未到刻度线,继续加水至刻度线
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源:2016届湖北省松滋市高三上学期期中测试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.将Ca(OH)2饱和溶液加热,溶液的pH增大
B.常温下,pH=11的氨水与pH=3的盐酸等体积混合后,溶液的pH>7
C.将0.1mol/L的HI溶液加水稀释l00倍,溶液中所有离子的浓度随之减小
D.两种醋酸溶液的pH分别为a和(a + 1),物质的量浓度分别为c1和c2,则有c1=10c2
查看答案和解析>>
科目:高中化学 来源:2016届江苏省苏北四市高三上学期期中质量抽测化学试卷(解析版) 题型:选择题
下列说法正确的是
A.在化学反应中,原子重新组合时伴随着能量的变化
B.淀粉和纤维素的化学式均为(C6H10O5)n,故互为同分异构体
C.通过化学变化可以“点石成金”,即可将黏土转化成金单质
D.等质量的铝粉按a、b两种途径完全转化,途径a比途径b消耗更多的NaOH
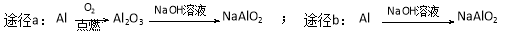
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一上学期10月月考化学试卷(解析版) 题型:选择题
1 L 1 mol·L-1 Na2SO4溶液中,下列各量正确的是
A.c(Na+)=1 mol·L-1 B.n(Na+)=3 mol
C.c(SO42-)=2 mol·L-1 D.m(Na2SO4)=142 g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一上学期10月月考化学试卷(解析版) 题型:选择题
下列关于溶液和胶体的叙述,正确的是
A.溶液是电中性的,胶体是带电的
B.通电时,溶液中的溶质粒子分别向两极移动,胶体中的分散质粒子向某一极移动
C.溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动
D.一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省杭州地区七校高一上学期期中联考化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数,下列说法正确的是
A. 2g氢气所含原子数目为NA
B. 标准状况下,11.2L H2O所含分子数为0.5NA
C. 1mol•L-1 CaCl2溶液中所含Ca2+离子的数目为NA
D. 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省杭州地区七校高一上学期期中联考化学试卷(解析版) 题型:选择题
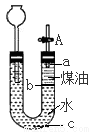
按如图所示实验装置进行钠跟水反应的实验,据此判断下列说法正确的是
A.
 打开右端胶塞,将一小块金属钠加入到煤油中,反应前片刻,钠的位置应在a处
打开右端胶塞,将一小块金属钠加入到煤油中,反应前片刻,钠的位置应在a处
B.开始反应后,能观察到的 实验现象是钠在b处液面以下的水中反应
实验现象是钠在b处液面以下的水中反应
C.反应一段时间后,左端液面上升,进入长颈漏斗,a处有无色气体产生
D.若用酒精来代替煤油,可观察到相同的实验现象
查看答案和解析>>
科目:高中化学 来源:2016届广东省高三上学期12月月考理综化学试卷(解析版) 题型:选择题
常温下,有关下列4种溶液的说法正确的是
① | ② | ③ | ④ |
0.1 mol·L-1氨水 | pH=11 氨水 | 0.1 mol·L-1盐酸 | pH=3 盐酸 |
A.由水电离出的c(H+):③>①
B.①稀释到原来的100倍,pH与②相同
C.①与③混合,若溶液pH=7,则溶液中c(NH4+)>c(Cl-)
D.②与④等体积混合,混合液pH>7
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江铁人中学高一上第一阶段测化学卷(解析版) 题型:实验题
(12分)用18 mol·L-1 浓硫酸配制100 mL 2.5 mol·L-1 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④转移 ⑤洗涤 ⑥定容 ⑦摇匀 完成下列问题:
(1)所需浓硫酸的体积是________(保留三位有效数字),量取浓硫酸所用的量筒的规格是________(从下列中选用A.10 mL B.25 mL C.50 mL D.100 mL)。
(2)该实验用到的仪器除量筒外还有 。
(3)第⑤步实验的操作是________________________________。
(4)第⑥步实验的操作是________________________________。
(5)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
①用量筒量取浓硫酸时俯视刻度___________________。
②容量瓶用蒸馏洗涤后未干燥________________。
③浓硫酸溶解后未冷却即转移、定容________________。
④定容时仰视刻度线________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com