
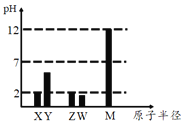
【题目】已知X、Y、Z、W、M 均为短周期元素。25℃时,其最高价氧化物对应的水化物(浓度均为0.01mol/L)溶液的pH和原子半径的关系如图所示。下列说法不正确的是
A.Z元素最高价氧化物的化学式为ZO3
B.简单离子半径大小顺序:X>M
C.简单气态氢化物的稳定性:Z>W>Y
D.X、Z的最简单气态氢化物反应有白烟生成
【答案】A
【解析】
X、Y、Z、W、M均为常见的短周期主族元素,由常温下,其最高价氧化物对应的水化物溶液(浓度均为 0.01mol/L)的pH,X的pH=2,为一元强酸,则为硝酸,X为N元素,Y的半径大于N,且酸性较硝酸弱,应为C元素;Z的原子半径大于C,Z的最高价含氧酸为一元强酸,则Z为Cl,W的原子半径大于Cl,且对应的酸的pH小于2,应为硫酸,W为S元素;M的原子半径最大,且0.01mol/L M的最高价氧化物对应的水化物溶液的pH为12,可知W为Na,以此解答该题。
由以上分析可知X、Y、Z、W、M分别为N、C、Cl、S、Na。
A. Z为Cl,最高化合价为+7价,最高价氧化物的化学式为Z2O7,故A错误;
B. X、M简单离子具有相同的核外电子排布,核电荷数越大,离子半径越小,则半径大小顺序:X>M,故B正确;
C. 非金属越强,简单气态氢化物稳定性越强,所以Cl>S>C,即Z>W>Y,故C正确;
D. X、Z的最简单气态氢化物反应生成氯化铵,有白烟生成,故D正确;
故选A。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】香草醛是一种食品添加剂,可由愈创木酚作原料合成,合成路线如图所示。下列说法正确的是( )
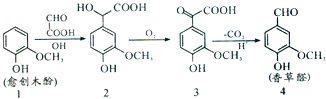
A.反应1→2中发生了取代反应
B.化合物2在一定条件下可发生缩聚反应
C.检验制得的香草醛中是否混有化合物3可用银氨溶液
D.等物质的量的四种化合物分别与足量H2反应,消耗H2物质的量之比为3:4:5:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向某浓度的二元弱酸H2C2O4溶液中逐滴加入NaOH溶液,pC与溶液pH的变化关系如图所示(pC=-lgx,x表示溶液中溶质微粒的物质的量浓度)。下列说法正确的是
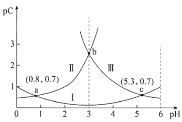
A.常温下,H2C2O4的Ka1=100.8
B.pH=3时,溶液中![]()
C.pH由0.8增大到5.3的过程中,水的电离程度逐渐增大
D.常温下,随着pH的增大,![]() 的值先增大后减小
的值先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84”消毒液、医用酒精等能对新冠病毒进行有效消杀。某兴趣小组在实验室自制“84”消毒液。请回答以下问题:
(1)“84”消毒液消杀新冠病毒的原理是__。
(2)甲同学设计图1所示实验装置(夹持装置省略)制取“84”消毒液。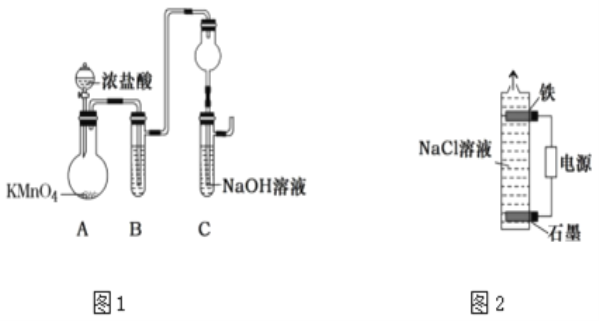
①B中的试剂是__。
②干燥管的作用是__。
③当C中NaOH溶液吸收完全后,停止通氯气,检验氯气已过量的方法为__。
(3)乙同学设计图2所示电解装置制取“84”消毒液。
①铁电极作__极。
②该电解制取NaClO的总反应的化学方程式为__。
③充分电解后,为检验电解液中是否还残留少量Cl-,取少量电解后溶液于试管中,滴加AgNO3溶液,试管中产生白色沉淀并有无色气体产生,该气体能使带火星的木条复燃。试管中发生反应的离子方程式为___。
④取25.00mL电解后溶液,加入过量KI与稀硫酸混合溶液,充分反应后加入2滴淀粉液,用0.1000molL-1Na2S2O3溶液滴定,消耗12.00mL。则该电解液有效氯(以有效氯元素的质量计算)的浓度为___mg/L。(已知:2S2O32-+I2═S4O62-+2I-)
(4)与甲同学制法相比,乙同学制法的优点除了有装置与操作简单外还有:__、__(请列举出两种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汉黄芩素是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有 关汉黄芩素的叙述正确的是
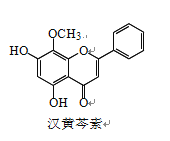
A. 汉黄芩素的分子式为 C16H13O5
B. 该物质遇 FeCl3 溶液显色
C. 1 mol 该物质与溴水反应,最多消耗 1 mol Br2
D. 与足量 H2 发生加成反应后,该分子中官能团的种类减少 1 种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际能源期刊报道了一种正在开发中的绿色环保“全氢电池”,有望减少废旧电池产生污染。其工作原理如图所示。下列说法正确的是
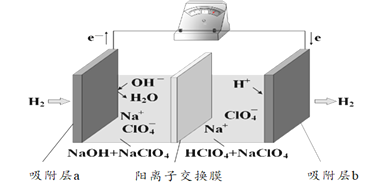
A.“全氢电池”工作时,将酸碱反应的中和能转化为电能
B.吸附层b发生的电极反应:H2 – 2e- + 2 OH-= 2H2O
C.Na+ 在装置中从右侧透过阳离子交换膜向左侧移动
D.“全氢电池”的总反应: 2H2 + O2 =2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组利用如图装置进行乙醇的催化氧化实验制取乙醛,图中铁架台等装置已略去,粗黑线表示乳胶管。请填写下列空白:
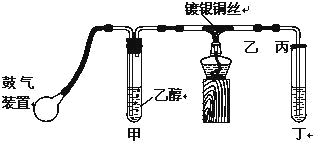
(1)甲装置常常浸在7080℃的水浴中,目的是___________
(2)实验时,先加热玻璃管乙中的镀银铜丝,约1分钟后鼓入空气,此时铜丝即呈红热状态。若把酒精灯撤走,控制一定的鼓气速度,铜丝能长时间保持红热直到实验结束。乙醇的催化氧化反应是__________反应(填“放热”或“吸热”),该反应的化学方程式为________
(3)该小组将丁中收集到的产物继续做实验探究:
①在试管中加入2毫升10%的_____溶液,在滴加四到五滴2%的_______溶液,配制成氢氧化铜悬浊液。然后加入丁中的产物,在酒精灯上加热,可以看到_________
②写出丁种物质与新制氢氧化铜反应的化学方程式___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】75号元素铼Re,熔点仅次于钨,是制造航空发动机的必需元素。地壳中铼的含量极低,多伴生于钼、铜、锌、铅等矿物中。回答下列问题:
(1)锰原子价层电子的轨道表示式为__,锰处于周期表的__区。
(2)与铼伴生的铜能形成多种配合物。如:醋酸二氨合铜(I)[Cu(NH3)2]Ac可用于吸收合成氨中对催化剂有害的CO气体:[Cu(NH3)2]Ac+CO+NH3![]() [Cu(NH3)3]Ac·CO。(Ac表示醋酸根)
[Cu(NH3)3]Ac·CO。(Ac表示醋酸根)
①与铜离子形成配合物的分子或离子应具备的结构特征是__。
②醋酸根中C原子的杂化类型为__,1mol配离子[Cu(NH3)2]+中含有σ键的数目为__。
③写出与NH3互为等电子体的一种离子的化学式__。
(3)锰与铼处于同一族,金属铼的熔点高于锰,原因是___。
(4)三氧化铼为立方晶胞,晶胞参数为apm,三氧化铼的摩尔质量为Mg/mol;铼原子占据顶点,氧原子占据所有棱心。则铼原子的配位数为__,铼原子填在了氧原子围成的空隙中___(填“四面体”“立方体”或“八面体”),三氧化铼的密度为__g/cm3。(用NA表示阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一份NaOH溶液在空气中放置较长时间后,与另一份新配制相同浓度的氢氧化钠溶液分别滴定相同体积、相同浓度的盐酸,能正确反映滴定过程中溶液pH变化曲线的是(虚线表示放置较长时间后的NaOH溶液,实线表示新配制的NaOH溶液)( )
A.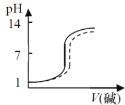 B.
B.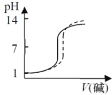 C.
C. D.
D.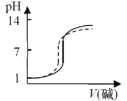
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com