
| A. | 浓HNO3 | B. | AgNO3 | C. | 氯水 | D. | 浓H2SO4 |
科目:高中化学 来源: 题型:选择题
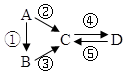
| A. | 若A是大气中含量最多的气体,C、D是氧化物且会造成光化学污染.则D转化成C的反应化学方程为3NO2+H2O=2HNO3+2NO | |
| B. | 若A、B、C分别为C(s)、CO(g)和CO2(g),且通过与O2(g)反应实现图示的转化.在同温同压且消耗含碳物质均为1mol时,反应①、②、③的焓变依次为△H1、△H 2、△H 3,则它们之间的关系为△H 2=△H1+△H 3 | |
| C. | 若C为一元强碱且阴、阳离子所含的电子数相同,D为日常生活中常用的调味品,工业上用D制备A的化学方程式2Na2O(熔融)$\frac{\underline{\;通电\;}}{\;}$4Na+O2↑ | |
| D. | 若A是应用最广泛的金属.④反应用到A,②、⑤反应均用到同一种气态非金属单质实验室保存D溶液的方法是加入适量铁粉与适量盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在0.2 mol•L-1的Na2CO3溶液中含有Na+的数目为0.4NA | |
| B. | 0.1 mol Fe参加氧化还原反应,转移的电子数目一定是0.3 NA | |
| C. | 15.6 g Na2O2 与过量CO2反应时,转移的电子数为0.4NA | |
| D. | 标准状况下22.4 L CH4和C2H4的混合气体所含氢原子数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑧⑩ | B. | ②④⑤⑥⑦⑨ | C. | ①②③④⑤ | D. | ⑥⑦⑧⑨⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中含有1mol Na2SO4 | |
| B. | 1L水中加入142g Na2SO4 | |
| C. | 1mol Na2SO4溶于1mol水中 | |
| D. | 将1mol Na2SO4溶于水后配成1L溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
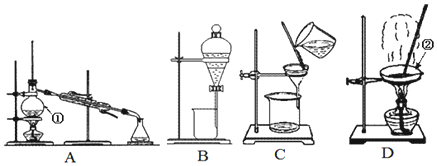
| A. | 烧瓶、锥形瓶、蒸发皿加热时均需要垫上石棉网 | |
| B. | 分液漏斗、滴定管、容量瓶使用前均需要检查是否漏水 | |
| C. | 配制1 mol•L-1NaCl溶液、测定Na2CO3溶液的pH、焰色反应实验均需要用到玻璃棒 | |
| D. | 量取25.00ml某盐酸,可以用量筒或者酸式滴定管 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯碱、烧碱、熟石灰、碱式碳酸铜都是碱 | |
| B. | 牛奶、豆浆、鸡蛋清溶液、食醋均为胶体 | |
| C. | H2SO4、NaOH、NaNO3、Na2O都是电解质 | |
| D. | 风化、钝化、皂化、焰色反应都是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com