
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1项 | B、2项 | C、3项 | D、4项 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、沸点H2O>HCl>HF |
| B、离子半径大小:S2->K+>Ca2+ |
| C、已知Ksp(AgCl)>Ksp(AgBr),则AgBr不可能转成AgCl |
| D、结合H+的能力:C6H5O->CO32->CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 甲 | 乙 |
| A | 1mol碳与足量浓硫酸反应 | 1mol铜与足量浓硫酸反应 |
| B | 1mol铁与足量稀硝酸反应 | 1mol铝与足量稀硝酸反应 |
| C | 27铝与足量氢氧化钠溶液反应 | 24g镁与足量盐酸反应 |
| D | 1L 12mol/L浓盐酸与足量MnO2反应 | 1L 12mol/L浓盐酸与足量KMnO4反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8[来源:www.shulihua.net] | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
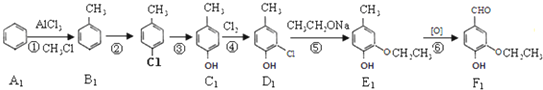
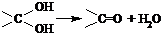 已知:
已知: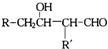
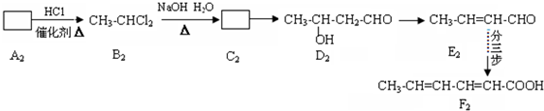
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com