
| Al的质量 |
| 镁铝合金质量 |
| 5.6L |
| 22.4L/mol |
|
| 2.7g |
| 5.1g |


 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
| A、2Mg+CO2=2MgO+C |
| B、2FeCl3+Fe=3 FeCl2 |
| C、SiO2+2C=Si+2CO↑ |
| D、Mg(OH)2+2HCl=MgCl2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
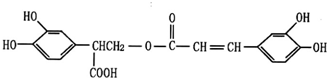

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
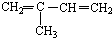 与Br2按物质的量之比1:1发生1,4加成反应方程式
与Br2按物质的量之比1:1发生1,4加成反应方程式查看答案和解析>>
科目:高中化学 来源: 题型:
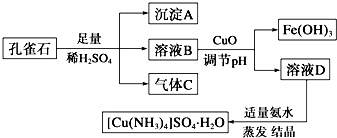
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、该反应能正向进行是因为正反应为熵增反应 |
| B、因为K在此温度下为气体,且采用真空抽走的方法,从反应体系中脱离,有利于反应的进行 |
| C、该反应说明了Na的还原性比K强 |
| D、该可逆反应为置换反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com