
分析 得到纯净的NaCl固体,除去可溶性杂质CaCl2、MgCl2和Na2SO4,选择NaOH除去MgCl2,选择BaCl2除去Na2SO4,选择Na2CO3除去CaCl2,且Na2CO3一定在BaCl2之后,过滤后加盐酸即可,以此来解答.
解答 解:得到纯净的NaCl固体,除去可溶性杂质CaCl2、MgCl2和Na2SO4,选择NaOH除去MgCl2,选择BaCl2除去Na2SO4,选择Na2CO3除去CaCl2,且Na2CO3一定在BaCl2之后,过滤后加盐酸即可,则顺序可为③②①⑤或②①③⑤或②③①⑤,过滤后得到的氯化钠溶液可在蒸发皿加热蒸发,得到氯化钠固体,
故答案为:③②①⑤或②①③⑤或②③①⑤;蒸发皿;蒸发.
点评 本题考查混合物分离提纯实验方案的设计,为高频考点,把握流程中的化学反应及混合物分离方法为解答的关键,侧重分析与实验能力、推断能力的考查,题目难度不大.


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 用加入适量NaCl溶液的方法除去Cu(NO3)2溶液中的AgNO3杂质 | |
| B. | 用洗气瓶中的NaOH溶液除去CO2气体中混有的HCl气体 | |
| C. | 分离FeCl3、KCl、BaSO4的固体混合物,应采用的一组试剂是:水、氢氧化钠、盐酸 | |
| D. | 先后添加石蕊试液、BaCl2溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 120℃,将wg甲醛在足量空气中燃烧,将生成产物用固体Na2O2(过量)吸收,固体增重wg | |
| B. | 24gMg带在足量CO2气体中燃烧,生成固体质量为40g | |
| C. | 相同物质的量的Al、Al2O3、Al(OH)3与足量NaOH溶液反应,溶液增重相等 | |
| D. | 在Fe3O4与足量浓硝酸的反应中,参加反应的Fe3O4与体现酸性的HNO3物质的量之比为1:10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
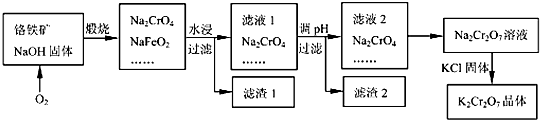
 Cr2O72-+H2O的存在,加稀硫酸增大了H+的浓度,平衡正向移动,使CrO42-浓度减小,Cr2O72-浓度增大,溶液由黄色变为橙色.
Cr2O72-+H2O的存在,加稀硫酸增大了H+的浓度,平衡正向移动,使CrO42-浓度减小,Cr2O72-浓度增大,溶液由黄色变为橙色.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH、Al--电解质 | B. | C2H4、O2--易燃气体 | ||
| C. | CaC2、K--遇湿易燃物品 | D. | KMnO4、KClO3--还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
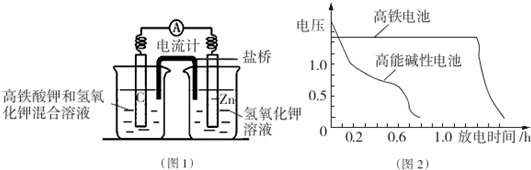
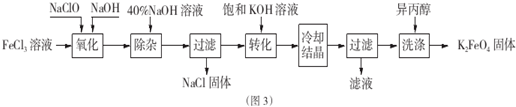
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com