
分析 能导电的物质必须有自由电子或自由移动的离子;
电解质是在水溶液里或熔融状态下能导电的化合物;
非电解质是在水溶液里和熔融状态下都不能导电的化合物.据此分析.
解答 解:(1)水银是金属,有自由移动的电子能导电;盐酸和硫酸溶液中有自由移动的离子能导电,故答案为:①⑤⑩;
(2)烧碱、氯化钠在水溶液或熔融状态能导电,液态氯化氢在水溶液中导电,属于电解质,故答案为:②④⑨;
(3)氨气的水溶液能导电,原因是氨气和水反应生成一水合氨,一水合氨能电离出自由移动的阴阳离子而使溶液导电,一水合氨是电解质,而氨气是非电解质;蔗糖在水溶液中和熔融状态下都不能能够导电的化合物,属于非电解质,故答案为:⑥⑦.
点评 本题考查电解质、非电解质的定义、物质导电的原因,题目难度不大,注意能导电的不一定是电解质,如水银、盐酸;电解质不一定能导电,如氯化钠晶体.


科目:高中化学 来源: 题型:推断题
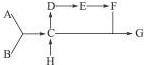 A、B、C、D、E、F、G、H八种物质间存在着如下图所示的变化关系,其中A、B为单质,相对分子质量A大于B;E在通常状况下为有颜色,有刺激性气味的气体;H为一种氯化物,与碱石灰共热可制取C;G中含A元素35%.
A、B、C、D、E、F、G、H八种物质间存在着如下图所示的变化关系,其中A、B为单质,相对分子质量A大于B;E在通常状况下为有颜色,有刺激性气味的气体;H为一种氯化物,与碱石灰共热可制取C;G中含A元素35%. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NF3中只含有极性共价键 | |
| B. | NF3既是氧化产物,又是还原产物 | |
| C. | NH4F中既含有离子键又含有共价键 | |
| D. | 上述反应中,反应物和生成物均属于共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯分子中共平面的原子最多是12个 | |
| B. | 对二甲苯分子中有4个碳原子在一条直线上 | |
| C. | 1-丁烯分子中的4个碳原子一定不在同一平面内 | |
| D. | 2-丁烯分子中的4个碳原子一定不在同一平面内 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na失火不能用CO2灭火,K失火也不能用CO2灭火 | |
| B. | Al与S直接化合可以得到Al2S3,Fe与S直接化合则得不到Fe2S3 | |
| C. | 将SO2通入BaCl2溶液中没有白色沉淀生成,将SO2通入Ba(NO3)2溶液中也没有白色沉淀生成 | |
| D. | CuSO4•5H2O投入浓H2SO4中,固体颜色由蓝变白 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热 | B. | 不用稀硫酸,改用98%浓硫酸 | ||
| C. | 加入硫酸铜 | D. | 不用铁片,改用铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验次数 | 初读数(mL) | 末读数(mL) |
| 1 | 0.00 | 18.50 |
| 2 | 0.00 | 22.45 |
| 3 | 0.00 | 18.48 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com