
某学习小组用如图所示装置测定铝镁合金中铝的质量分数和铝的相对原子质量。

(1)A中试剂为____________。
(2)实验前,先将铝镁合金在稀酸中浸泡片刻,其目的是____________________
__________________________________________________________________。
(3)检查气密性,将药品和水装入各仪器中,连接好装置后,需进行的操作还有:
①记录C的液面位置;
②将B中剩余固体过滤、洗涤、干燥、称重;
③待B中不再有气体产生并恢复至室温后,记录C的液面位置;
④由A向B滴加足量试剂;
⑤检查气密性。
上述操作的顺序是________(填序号);记录C的液面位置时,除视线平视外,还应____________。
(4)B中发生反应的化学方程式为______________________________________。
(5)若实验用铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),B中剩余固体的质量为cg,则铝的相对原子质量为________。
(6)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将________
(填“偏大”“偏小”或“无影响”)。
【解析】(1)观察实验装置图可知是用量气法完成实验目的,故A中应盛NaOH溶液,在B中发生2Al+2NaOH+2H2O====2NaAlO2+3H2↑的反应。
(2)目的是除去铝镁合金表面的氧化膜。
(3)正确顺序应为⑤①④③②;为使C中气体的压强与外界大气压相等,还应使D与C的液面相平。
(5)据2Al ~ 3H2
2 mol 3 mol
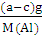
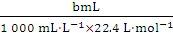
得M(Al)=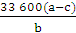
(6)据w(Al)=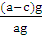 ×100%的计算公式可知未洗涤不溶物会造成铝的质量分数偏小。
×100%的计算公式可知未洗涤不溶物会造成铝的质量分数偏小。
答案:(1)NaOH溶液
(2)除去铝镁合金表面的氧化膜
(3)⑤①④③② 使D和C的液面相平
(4)2Al+2NaOH+2H2O====2NaAlO2+3H2↑
(5)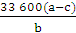 (6)偏小
(6)偏小


科目:高中化学 来源: 题型:
同种物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应是
( )
A.3Br2+6KOH====5KBr+KBrO3+3H2O
B.MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
C.2KNO3 2KNO2+O2↑
2KNO2+O2↑
D.NH4NO3 N2O↑+2H2O
N2O↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
从反应类型的角度来看,下列化学反应中,与其他三个类型不同的是( )
A.锌粒与稀硫酸反应制取氢气
B.铁粉投入硫酸铜溶液中析出铜
C.金属钠投入水中产生氢气和氢氧化钠
D.一氧化碳与三氧化二铁加热生成金属铁
查看答案和解析>>
科目:高中化学 来源: 题型:
两种金属粉末的混合物52 g,溶于足量的稀硫酸中,生成标准状况下的氢气22.4 L,则这种混合物不可能是( )
A.Na和K B.Mg和Al C.Cu和Al D.Al和Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素甲~戊在元素周期表中的相对位置如表所示,下面判断正确的是( )
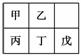
A.原子半径:丙<丁<戊
B.金属性:甲>丙
C.氢氧化物碱性:丙>丁>戊
D.最外层电子数:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
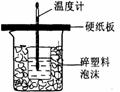 (1) 从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间 满碎塑料泡沫的作用是______________________________________________。
(1) 从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间 满碎塑料泡沫的作用是______________________________________________。
(2) 大烧杯上如不盖硬纸板,则求得的中和热数值_______
(填“偏大”、“偏小”、“无影响”)
(3) 实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,与上述实验相比,溶液温度升高度数________(填“相等”或“不相等”)。所求中和热的数值会________(填“相等”或“不相等”),理由是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
根据元素周期表1~20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有________种,金属性最强的元素与氧反应生成的化合物有________(填两种化合物的化学式)。
(2)属于稀有气体的是________(填元素符号,下同);
(3)形成化合物种类最多的两种元素是________;
(4)第3周期中,原子半径最大的是(稀有气体除外)________;
(5)推测Si、N最简单氢化物的稳定性:________大于________(填化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com