
A、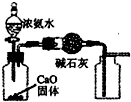 如图用装置制取并收集干燥纯净的NH3 |
B、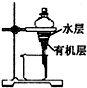 如图用装置分离苯萃取碘水后已分层的有机层和水层 |
C、 如图用装置配制一定的物质的量浓度的稀硫酸 |
D、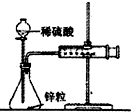 如图用装置测定锌与稀硫酸反应的速率 |


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaOH溶液 |
| △ |
| 酸性K2Cr2O7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 合成氨是人类科学技术发展史上的一项重大突破,解决了地球上因粮食不足而导致的饥饿与死亡.
合成氨是人类科学技术发展史上的一项重大突破,解决了地球上因粮食不足而导致的饥饿与死亡.查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 灼烧一小块铝箔 | 熔化的铝并不滴落 | Al2O3的熔点高于Al |
| B | 用洁净的铂丝蘸取某化合物少许,放在酒精灯外焰上灼烧 | 火焰呈黄色 | 该化合物中一定含钠元素 |
| C | 向溶液中滴加盐酸酸化的氯化钡溶液 | 有白色沉淀产生 | 该溶液一定含有SO42-离子 |
| D | 向KMnO4酸性溶液中滴加草酸溶液 | 紫红色褪去 | 草酸具有还原性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、二糖 | B、多糖 | C、氨基酸 | D、脂肪 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com