
水热法制备Fe(FeO2)2纳米颗粒的反应3Fe2++2S2O32-+O2+xOH-=Fe(FeO2)2+S4O62-+2H2O,下列说法中不正确的是
A.每生成1molFe(FeO2)2转移4mol电子
B.该反应中Fe2+和S2O32-都是还原剂
C.3molFe2+被氧化时有1molO2被还原
D.反应方程式中化学计量数x=4
科目:高中化学 来源:2016-2017年新疆兵团第二师华山中学高二上学前考化学卷(解析版) 题型:选择题
应用元素周期律分析下列推断,其中正确的组合是
①碱金属单质的熔点随原子序数的增大而降低
②砹(At)是第VIIA族,其氢化物的稳定性大于HCl
③硒(Se)的最高价氧化物对应水化物的酸性比硫酸弱
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤铊(Tl)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
⑥第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱
A. ①③④ B. ①③⑥ C. ③④⑤ D. ②④⑥
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆实验中学高一上开学考化学卷(解析版) 题型:选择题
室温时,将氢氧化钠溶液与盐酸用滴加方式反应时,溶液的pH随滴入溶液体积变化如图所示,下列有关说法不正确的是
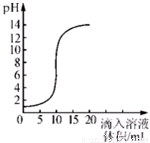
A.该图象表示的是将氢氧化钠溶液滴入盐酸中
B.氢氧化钠溶液和盐酸恰好完全反应时.溶液的pH等于7
C.当滴入溶液的体积为5mL时,所得溶液中的溶质只有NaCl
D.滴入溶液体积为15mL时,再加几滴紫色石蕊试液溶液呈蓝色
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上学期第一次月考化学试卷(解析版) 题型:推断题
艾薇醛(G,分子式:C9H14O)是一种新型的香料,可通过下列途径合成。

已知下列信息:
①A的核磁共振氢谱有3组峰,峰面积比为6:3:1
②A、C、F均能使Br2/CCl4溶液褪色
③D、E、F、G1、G2均能发生银镜反应,F中含甲基
④Diels-Alder反应(双烯合成反应)。如:
⑤
回答下列问题:
(1)A的名称为 ;E→F的反应类型是 。
(2)B→C的化学方程式为 。
(3)D的结构简式为 。
(4)G1、G2(均含六元环)互为同分异构体,其结构简式分别为 ;
G1、G2在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是 (填标号)
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪
(5)与E互为同分异构体且能发生银镜反应的异构体有 种(不含立体结构,不含醚键),其中核磁共振氢谱有3组峰且面积比为6:1:1的结构简式为 。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上学期第一次月考化学试卷(解析版) 题型:选择题
2015年10月,屠呦呦获得诺贝尔生理学或医学奖,理由是她发现了青蒿素,这种药品可以有效降低疟疾患者的死亡率。她成为首获科学类诺贝尔奖的中国人。青蒿素两步可合成得到治疗疟疾的药物青蒿琥酯。下列有关说法正确的是
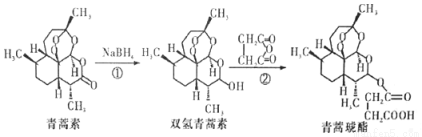
A.青蒿素分子式为C15H24O5
B.反应②原子利用率为100%
C.该过程中青蒿素生成双氢青蒿素属于氧化反应
D.1mol青蒿琥酯与氢氧化钠溶液反应,最多消耗1mol氢氧化钠
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.可使用溴水鉴别植物油和汽油
B.利用二氧化碳制造可降解塑料,可以消除温室效应
C.“玉兔号”月球车上的太阳能电池的材料是硅
D.实验室金属钠失火时,可使用泡沫灭火器灭火
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上开学考化学试卷(解析版) 题型:选择题
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是

A.该反应的化学方程式为3B+4D 6A+2C
6A+2C
B.反应进行到1 s时,v(A)=v(D)
C.反应进行到6 s时,B的平均反应速率为0.05 mol/(L·s)
D.反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源:2017届广西省高三上8月月考理综化学试卷(解析版) 题型:推断题
选修X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大.X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子的未成对电子数在同周期元素中最多,W形成的单质是空气的主要成分之一, R与Y同一主族,Q的最外层只有一个电子,其他电子层电子均处于饱和状态。请回答下列问题:

(1)Q+核外电子排布式为___________;
(2)化合物YX4中Y的杂化方式为__________,ZW3-离子的立体构型是_______。
(3)Y、R的最高价氧化物的沸点较高的是_______(填化学式),原因是____________。
(4)Q元素可形成一种化合物[Q(NH3)4]SO4,该物质中含化学键有________。
(5)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图,该晶体一个晶胞的Y原子数为________,Y原子的配位数为_______,若晶胞的边长为a nm,晶体的密度为ρg/cm3,则阿伏加德罗常数的数值为____________(用含a和ρ的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com