
”¾ĢāÄæ”æ·ēĆŅČ«ĒņµÄŅūĮĻ¹ū“×ÖŠŗ¬ÓŠĘ»¹ūĖį£ØMLA£©£¬Ęä·Ö×ÓŹ½ĪŖC4H6O5”£0.1molĘ»¹ūĖįÓė×ćĮæµÄNaHCO3ČÜŅŗ·“Ó¦ÄܲśÉś4.48LCO2£Ø±ź×¼×“æö£©£¬Ę»¹ūĖįĶŃĖ®ÄÜÉś³ÉŹ¹äåĖ®ĶŹÉ«µÄ²śĪļ”£Ę»¹ūĖį¾¾ŪŗĻÉś³É¾ŪĘ»¹ūĖįõ„£ØPMLA£©”£
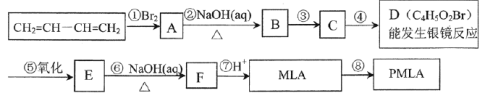
£Ø1£©Š“³öĪļÖŹµÄ½į¹¹¼ņŹ½£ŗA___£¬D___”£
£Ø2£©Öø³öŗĻ³ÉĀ·ĻßÖŠ¢Ł”¢¢ŚµÄ·“Ó¦ĄąŠĶ£ŗ¢Ł___£»¢Ś___”£
£Ø3£©Š“³öĖłÓŠÓėMLA¾ßÓŠĻąĶ¬¹ŁÄÜĶŵÄĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½£ŗ___”£
£Ø4£©Š“³öE”śF×Ŗ»ÆµÄ»Æѧ·½³ĢŹ½___”£
£Ø5£©ÉĻŹö×Ŗ»Æ¹ŲĻµÖŠ²½Öč¢ŪŗĶ¢ÜµÄĖ³ŠņÄÜ·ńµßµ¹?___£ØĢī”°ÄÜ”±»ņ”°²»ÄÜ”±£©”£ĖµĆ÷ĄķÓÉ£ŗ___”£
£Ø6£©ĒėŠ“³öŅŌ±ūĻ©ĪŖŌĮĻÖʱøČéĖį£Ø2-ōĒ»ł±ūĖį£©µÄŗĻ³ÉĀ·ĻßĮ÷³ĢĶ¼£ØĪŽ»śŹŌ¼ĮČĪČ”£©___”£
”¾“š°ø”æCH2BrCH=CHCH2Br OHCCH2CHBrCHO ¼Ó³É·“Ó¦ Č”“ś£ØĖ®½ā£©·“Ó¦ ![]() ”¢
”¢ HOOCCH2CHBrCOOH+3NaOH”śNaOOCCH2CH(OH)COONa+NaBr+2H2O ²»ÄÜ ČōĻČŃõ»ÆŌņBÖŠĢ¼Ģ¼Ė«¼üŅ²±»Ńõ»Æ
HOOCCH2CHBrCOOH+3NaOH”śNaOOCCH2CH(OH)COONa+NaBr+2H2O ²»ÄÜ ČōĻČŃõ»ÆŌņBÖŠĢ¼Ģ¼Ė«¼üŅ²±»Ńõ»Æ ![]()
”¾½āĪö”æ
Ę»¹ūĖį·Ö×ÓŹ½ĪŖ![]() £¬
£¬![]() molĘ»¹ūĖįÓė×ćĮæ
molĘ»¹ūĖįÓė×ćĮæ![]() ČÜŅŗ·“Ó¦ÄܲśÉś
ČÜŅŗ·“Ó¦ÄܲśÉś![]()
![]() ±ź×¼×“æö
±ź×¼×“æö![]() £¬¶žŃõ»ÆĢ¼µÄĪļÖŹµÄĮæĪŖ
£¬¶žŃõ»ÆĢ¼µÄĪļÖŹµÄĮæĪŖ![]() £¬Ōņ1molĘ»¹ūĖįŗ¬
£¬Ōņ1molĘ»¹ūĖįŗ¬![]() Ę»¹ūĖįĶŃĖ®ÄÜÉś³ÉŹ¹äåĖ®ĶŹÉ«µÄ²śĪļ£¬Ó¦ŗ¬ÓŠ1øö
Ę»¹ūĖįĶŃĖ®ÄÜÉś³ÉŹ¹äåĖ®ĶŹÉ«µÄ²śĪļ£¬Ó¦ŗ¬ÓŠ1øö![]() £¬½įŗĻĘ»¹ūĖįµÄ·Ö×ÓŹ½ÖŖ£¬Ę»¹ūĖįµÄ½į¹¹¼ņŹ½ĪŖ£ŗ
£¬½įŗĻĘ»¹ūĖįµÄ·Ö×ÓŹ½ÖŖ£¬Ę»¹ūĖįµÄ½į¹¹¼ņŹ½ĪŖ£ŗ![]() ”£Ę»¹ūĖįõ„»Æ·“Ó¦½ųŠŠµÄ¾ŪŗĻÉś³É¾ŪĘ»¹ūĖį
”£Ę»¹ūĖįõ„»Æ·“Ó¦½ųŠŠµÄ¾ŪŗĻÉś³É¾ŪĘ»¹ūĖį![]() £¬Ęä½į¹¹ĪŖ
£¬Ęä½į¹¹ĪŖ![]() ”£D±»Ńõ»ÆÉś³ÉE£¬ŌņEÖŠŗ¬ÓŠäåŌ×Ó£¬EŗĶĒāŃõ»ÆÄʵÄĖ®ČÜŅŗ·¢Éś·“Ӧɜ³ÉF£¬FĖį»ÆÉś³ÉMLA£¬ĖłŅŌFµÄ½į¹¹¼ņŹ½ĪŖ£ŗ
”£D±»Ńõ»ÆÉś³ÉE£¬ŌņEÖŠŗ¬ÓŠäåŌ×Ó£¬EŗĶĒāŃõ»ÆÄʵÄĖ®ČÜŅŗ·¢Éś·“Ӧɜ³ÉF£¬FĖį»ÆÉś³ÉMLA£¬ĖłŅŌFµÄ½į¹¹¼ņŹ½ĪŖ£ŗ![]() £¬EµÄ½į¹¹¼ņŹ½ĪŖ£ŗ
£¬EµÄ½į¹¹¼ņŹ½ĪŖ£ŗ![]() £¬DÄÜ·¢ÉśŅų¾µ·“Ó¦ŌņDÖŠŗ¬ÓŠČ©»ł£¬ĖłŅŌDµÄ½į¹¹¼ņŹ½ĪŖ£ŗ
£¬DÄÜ·¢ÉśŅų¾µ·“Ó¦ŌņDÖŠŗ¬ÓŠČ©»ł£¬ĖłŅŌDµÄ½į¹¹¼ņŹ½ĪŖ£ŗ![]() £¬øł¾Ż1£¬
£¬øł¾Ż1£¬![]() ¶”¶žĻ©¼°DµÄ½į¹¹¼ņŹ½ÖŖ£¬1£¬
¶”¶žĻ©¼°DµÄ½į¹¹¼ņŹ½ÖŖ£¬1£¬![]() ¶”¶žĻ©ŗĶäå·¢Éś1£¬4¼Ó³ÉÉś³ÉAĪŖ
¶”¶žĻ©ŗĶäå·¢Éś1£¬4¼Ó³ÉÉś³ÉAĪŖ![]() £¬AŗĶĒāŃõ»ÆÄʵÄĖ®ČÜŅŗ·¢ÉśČ”“ś·“Ӧɜ³ÉBĪŖ
£¬AŗĶĒāŃõ»ÆÄʵÄĖ®ČÜŅŗ·¢ÉśČ”“ś·“Ӧɜ³ÉBĪŖ![]() £¬BÓėHBr·¢Éś¼Ó³É·“Ӧɜ³ÉC£¬CµÄ½į¹¹¼ņŹ½ĪŖ£ŗ
£¬BÓėHBr·¢Éś¼Ó³É·“Ӧɜ³ÉC£¬CµÄ½į¹¹¼ņŹ½ĪŖ£ŗ![]() £¬CŌŁ±»Ńõ»ÆÉś³ÉD£¬Ę»¹ūĖį¾¾ŪŗĻÉś³É¾ŪĘ»¹ūĖį
£¬CŌŁ±»Ńõ»ÆÉś³ÉD£¬Ę»¹ūĖį¾¾ŪŗĻÉś³É¾ŪĘ»¹ūĖį![]() £¬¾Ż“Ė½ā“š”£
£¬¾Ż“Ė½ā“š”£
![]() ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬AĪŖ
ÓÉÉĻŹö·ÖĪöæÉÖŖ£¬AĪŖ![]() £¬DĪŖ
£¬DĪŖ![]() £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ![]() £»
£»![]() £»
£» ![]() ·“Ó¦
·“Ó¦![]() ŹĒ1£¬
ŹĒ1£¬![]() ¶”¶žĻ©ŗĶäå·¢Éś1£¬4¼Ó³ÉÉś³É
¶”¶žĻ©ŗĶäå·¢Éś1£¬4¼Ó³ÉÉś³É![]() £¬·“Ó¦
£¬·“Ó¦![]() ŹĒ
ŹĒ![]() ŗĶĒāŃõ»ÆÄʵÄĖ®ČÜŅŗ·¢ÉśČ”“ś·“Ӧɜ³É
ŗĶĒāŃõ»ÆÄʵÄĖ®ČÜŅŗ·¢ÉśČ”“ś·“Ӧɜ³É![]() £¬¹Ź“š°øĪŖ£ŗ¼Ó³É·“Ó¦£»Č”“ś·“Ó¦£»
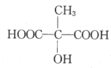
£¬¹Ź“š°øĪŖ£ŗ¼Ó³É·“Ó¦£»Č”“ś·“Ó¦£» ![]() ĖłÓŠÓėMLA¾ßÓŠĻąĶ¬¹ŁÄÜĶŵÄĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½ÓŠ£ŗ
ĖłÓŠÓėMLA¾ßÓŠĻąĶ¬¹ŁÄÜĶŵÄĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½ÓŠ£ŗ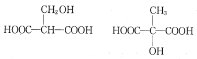 £¬ ¹Ź“š°øĪŖ£ŗ
£¬ ¹Ź“š°øĪŖ£ŗ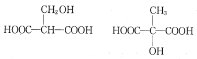 £»
£» ![]() ×Ŗ»ÆµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ
×Ŗ»ÆµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ![]() £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ![]() £»
£» ![]() Ė³Šņ²»Äܵߵ¹£¬ČōĻČŃõ»ÆŌņBÖŠĢ¼Ģ¼Ė«¼üŅ²±»Ńõ»Æ£¬¹Ź“š°øĪŖ£ŗ²»ÄÜ£¬ČōĻČŃõ»ÆŌņBÖŠĢ¼Ģ¼Ė«¼üŅ²±»Ńõ»Æ£»
Ė³Šņ²»Äܵߵ¹£¬ČōĻČŃõ»ÆŌņBÖŠĢ¼Ģ¼Ė«¼üŅ²±»Ńõ»Æ£¬¹Ź“š°øĪŖ£ŗ²»ÄÜ£¬ČōĻČŃõ»ÆŌņBÖŠĢ¼Ģ¼Ė«¼üŅ²±»Ńõ»Æ£»
(6) ±ūĻ©ŗĶHOBr·¢Éś¼Ó³É·“Ӧɜ³ÉCH3CHBrCH2OH£¬CH3CHBrCH2OH·¢ÉśŃõ»Æ·“Ӧɜ³ÉCH3CHBrCOOH£¬CH3CHBrCOOHŗĶĒāŃõ»ÆÄʵÄĖ®ČÜŅŗ¼ÓČČĖį»ÆµĆµ½CH3CHOHCOOH£¬¹Ź“š°øĪŖ£ŗ![]() ”£
ӣ


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ·“Ó¦¢Ł£ŗCO(g)£«CuO(s) ![]() CO2(g)£«Cu(s)ŗĶ·“Ó¦¢Ś£ŗH2(g)£«CuO(s)
CO2(g)£«Cu(s)ŗĶ·“Ó¦¢Ś£ŗH2(g)£«CuO(s) ![]() Cu(s)£«H2O(g)ŌŚĻąĶ¬µÄijĪĀ¶ČĻĀµÄĘ½ŗā³£Źż·Ö±šĪŖK1ŗĶK2£¬øĆĪĀ¶ČĻĀ·“Ó¦¢Ū£ŗCO(g)£«H2O(g)
Cu(s)£«H2O(g)ŌŚĻąĶ¬µÄijĪĀ¶ČĻĀµÄĘ½ŗā³£Źż·Ö±šĪŖK1ŗĶK2£¬øĆĪĀ¶ČĻĀ·“Ó¦¢Ū£ŗCO(g)£«H2O(g) ![]() CO2(g)£«H2(g)µÄĘ½ŗā³£ŹżĪŖK”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(”” ””)
CO2(g)£«H2(g)µÄĘ½ŗā³£ŹżĪŖK”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(”” ””)
A.·“Ó¦¢ŁµÄĘ½ŗā³£ŹżK1£½![]()
B.·“Ó¦¢ŪµÄĘ½ŗā³£ŹżK£½![]()
C.¶ŌÓŚ·“Ó¦¢Ū£¬ŗćČŻŹ±£¬ĪĀ¶ČÉżøߣ¬H2ÅØ¶Č¼õŠ”£¬ŌņøĆ·“Ó¦ĪŖĪüČČ·“Ó¦
D.¶ŌÓŚ·“Ó¦¢Ū£¬ŗćĪĀŗćČŻĻĀ£¬Ōö“óŃ¹Ē棬H2ÅضČŅ»¶ØŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ500”ꏱ£¬ŌŚĖÄøöĢå»żĪŖ2LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗNO2(g) + SO2(g)![]() SO3(g)+ NO(g)”£ÓŠ¹ŲĪļÖŹĘšŹ¼Ź±µÄĪļÖŹµÄĮæŹż¾ŻČēĻĀ±ķĖłŹ¾£ŗ
SO3(g)+ NO(g)”£ÓŠ¹ŲĪļÖŹĘšŹ¼Ź±µÄĪļÖŹµÄĮæŹż¾ŻČēĻĀ±ķĖłŹ¾£ŗ
ČŻĘ÷ | ĘšŹ¼Ź±ĪļÖŹµÄĮæ/mol | |||
NO2 | SO2 | SO3 | NO | |
¼× | 0.1 | 0.1 | 0 | 0 |
ŅŅ | 0.15 | 0.05 | 0.05 | 0.05 |
±ū | 0 | 0 | 0.2 | 0.2 |
¶” | 0.1 | 0.2 | 0 | 0 |
ŅŃÖŖ¼×ČŻĘ÷“ļµ½Ę½ŗāŹ±ČŻĘ÷ÖŠc(SO3)=0.01mol”¤L£1”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A.ÉżĪĀÖĮ700”ę£¬ÉĻŹö·“Ó¦µÄĘ½ŗā³£ŹżĪŖ![]() £¬ŌņÕż·“Ó¦ĪŖĪüČČ·“Ó¦
£¬ŌņÕż·“Ó¦ĪŖĪüČČ·“Ó¦
B.“ļĘ½ŗāŹ±£¬ČŻĘ÷±ūÖŠc(SO2)ŹĒČŻĘ÷¼×µÄ2±¶
C.“ļĘ½ŗāŹ±£¬ČŻĘ÷¶”ÖŠc(NO)ÓėŅŅČŻĘ÷ÖŠĻąĶ¬
D.±£³ÖĪĀ¶Č²»±äČŻĘ÷¼×“ļµ½Ę½ŗāŹ±ŌŁ³äČėSO2(g)ŗĶSO3(g)ø÷0.02mol£¬“ĖŹ±v(Õż)£¾v(Äę)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆH2O2ŗĶH2SO4µÄ»ģŗĻČÜŅŗæÉøÆŹ“Ó”Ė¢µēĀ·°åÉĻµÄĶ£¬ĘäČČ»Æѧ·½³ĢŹ½ĪŖCu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l) ¦¤H
ŅŃÖŖ¢ŁCu(s)+2H+(aq)=Cu2+(aq)+H2(g) ¦¤H1=64kJ”¤mol-1
¢Ś2H2O2(l)=2H2O(l)+O2(g) ¦¤H2=-196kJ”¤mol-1
¢ŪH2(g)+![]() O2(g)=H2O(l) ¦¤H3=-286kJ”¤mol-1
O2(g)=H2O(l) ¦¤H3=-286kJ”¤mol-1
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
A.·“Ó¦¢ŁæÉĶعżĶ×÷µē¼«µē½āĻ”µÄH2SO4·½·ØŹµĻÖ
B.·“Ó¦¢ŚŌŚČĪŗĪĢõ¼žĻĀ¶¼ÄÜ×Ō·¢½ųŠŠ
C.ČōH2(g)+![]() O2(g)=H2O(g) ¦¤H4£¬Ōņ¦¤H4£¼¦¤H3
O2(g)=H2O(g) ¦¤H4£¬Ōņ¦¤H4£¼¦¤H3
D.¦¤H=-320kJ”¤mol-1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æµŖŌŖĖŲµÄ»ÆŗĻĪļŌŚ¹¤Å©ŅµŅŌ¼°¹ś·ĄæĘ¼¼ÖŠÓĆĶ¾¹ć·ŗ£¬µ«Ņ²»į¶Ō»·¾³Ōģ³ÉĪŪČ¾£¬ČēµŲĻĀĖ®ÖŠĻõĖįŃĪŌģ³ÉµÄµŖĪŪČ¾ŅŃ³ÉĪŖŅ»øöŹĄ½ēŠŌµÄ»·¾³ĪŹĢā”£
£Ø1£©ÉńÖŪŌŲČĖ·É“¬µÄ»š¼żĶĘ½ųĘ÷ÖŠ³£ÓĆėĀ£ØN2H4£©×÷Č¼ĮĻ”£NH3ÓėNaClO·“Ó¦æɵƵ½ėĀ£ØN2H4£©£¬øĆ·“Ó¦ÖŠ±»Ńõ»ÆÓė±»»¹ŌµÄŌŖĖŲµÄŌ×ÓøöŹżÖ®±ČĪŖ___”£Čē¹ū·“Ó¦ÖŠÓŠ5molµē×Ó·¢Éś×ŖŅĘ£¬æɵƵ½___ gėĀ”£
£Ø2£©³£ĪĀĻĀĻņ25mL0.01mol/LĻ”ŃĪĖįÖŠ»ŗ»ŗĶØČė5.6mLNH3£Ø±ź×¼×“æö£¬ČÜŅŗĢå»ż±ä»ÆŗöĀŌ²»¼Ę£©£¬·“Ó¦ŗóČÜŅŗÖŠĄė×ÓÅضČÓɓ󵽊”µÄĖ³ŠņŹĒ___”£ŌŚĶØČėNH3µÄ¹ż³ĢÖŠČÜŅŗµÄµ¼µēÄÜĮ¦___£ØĢīŠ“”°±ä“ó”±”¢”°±äŠ””±»ņ”°¼øŗõ²»±ä”±£©”£
£Ø3£©ĻņÉĻŹöČÜŅŗÖŠ¼ĢŠųĶØČėNH3£¬øĆ¹ż³ĢÖŠĄė×ÓÅØ¶Č“óŠ”¹ŲĻµæÉÄÜÕżČ·µÄŹĒ___£ØŃ”Ģī±ąŗÅ£©”£
a£®[Cl-]=[NH4+]£¾[H+]=[OH-] b£®[Cl-]£¾[NH4+]=[H+]£¾[OH-
c£®[NH4+]£¾[OH-]£¾[Cl-]£¾[H+] d£®[OH-]£¾[NH4+]£¾[H+]£¾[Cl-]
£Ø4£©³£ĪĀĻĀĻņ25mLŗ¬HCl0.01molµÄČÜŅŗÖŠµĪ¼Ó°±Ė®ÖĮ¹żĮ棬øĆ¹ż³ĢÖŠĖ®µÄµēĄėĘ½ŗā£ØĢīŠ“µēĄėĘ½ŗāŅʶÆĒéæö£©___”£µ±µĪ¼Ó°±Ė®µ½25mLŹ±£¬²āµĆČÜŅŗÖŠĖ®µÄµēĄė¶Č×ī“ó£¬Ōņ°±Ė®µÄÅضČĪŖ___mol”¤L-1”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃé²»ÄÜ“ļµ½Ō¤ĘŚÄæµÄŹĒ£Ø””””£©
ŹµŃé²Ł×÷ | ŹµŃéÄæµÄ | |
A | ³äĀśNO2µÄĆܱղ£Į§Ēņ·Ö±š½žÅŻŌŚĄä”¢ČČĖ®ÖŠ | ŃŠ¾æĪĀ¶Č¶Ō»ÆŃ§Ę½ŗāŅĘ¶ÆµÄÓ°Ļģ |
B | ĻņŹ¢ÓŠ1mLĻõĖįŅųČÜŅŗµÄŹŌ¹ÜÖŠµĪ¼ÓNaClČÜŅŗ£¬ÖĮ²»ŌŁÓŠ³Įµķ£¬ŌŁĻņĘäÖŠµĪ¼ÓNa2SČÜŅŗ | ĖµĆ÷Ņ»ÖÖ³ĮµķÄÜ×Ŗ»ÆĪŖĮķŅ»ÖÖČܽā¶ČøüŠ”µÄ³Įµķ |
C | ±½·ÓŗĶĖ®µÄ×ĒŅŗÖŠ£¬¼ÓÉŁĮæÅØĢ¼ĖįÄĘČÜŅŗ | ±Č½Ļ±½·ÓÓėĢ¼ĖįĒāÄʵÄĖįŠŌ |
D | ȔɣĮæČÜŅŗµĪ¼ÓCa£ØOH£©2ČÜŅŗ£¬¹Ū²ģŹĒ·ń³öĻÖ°×É«»ė×Ē | Č·¶ØNaHCO3ČÜŅŗÖŠŹĒ·ń»ģÓŠNa2CO3 |
A.AB.BC.CD.D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ![]() ”¢
Ӣ![]() Ӣ
Ӣ![]() Ӣ
Ӣ![]() Ӣ
”¢![]() ¾łŹĒ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČēĶ¼ĖłŹ¾£¬ĘäÖŠ
¾łŹĒ¶ĢÖÜĘŚŌŖĖŲ£¬ĖüĆĒŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĻą¶ŌĪ»ÖĆČēĶ¼ĖłŹ¾£¬ĘäÖŠ![]() Óė
Óė![]() ŠĪ³ÉµÄŅ»ÖÖ»ÆŗĻĪļÄÜŹ¹Ę·ŗģČÜŅŗĶŹÉ«£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
ŠĪ³ÉµÄŅ»ÖÖ»ÆŗĻĪļÄÜŹ¹Ę·ŗģČÜŅŗĶŹÉ«£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©

A.![]() Óė
Óė![]() ŠĪ³ÉµÄĮ½ÖÖ³£¼ū»ÆŗĻĪļÖŠŗ¬ÓŠµÄ»Æѧ¼üĄąŠĶČ«²æĻąĶ¬
ŠĪ³ÉµÄĮ½ÖÖ³£¼ū»ÆŗĻĪļÖŠŗ¬ÓŠµÄ»Æѧ¼üĄąŠĶČ«²æĻąĶ¬
B.æÉÓĆ![]() ČÜŅŗ³żČ„
ČÜŅŗ³żČ„![]() µ„ÖŹÖŠ»ģÓŠµÄ
µ„ÖŹÖŠ»ģÓŠµÄ![]() µ„ÖŹ
µ„ÖŹ
C.¼ņµ„Ēā»ÆĪļµÄČČĪČ¶ØŠŌ£ŗ![]()
D.»ÆŗĻĪļ![]() ŗĶ
ŗĶ![]() ÖŠ£¬ŃōĄė×Ó°ė¾¶¾ł“óÓŚŅõĄė×Ó°ė¾¶
ÖŠ£¬ŃōĄė×Ó°ė¾¶¾ł“óÓŚŅõĄė×Ó°ė¾¶
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠĮ½ÖÖĘųĢ¬µ„ÖŹ![]() ŗĶ
ŗĶ![]() £¬ŅŃÖŖ
£¬ŅŃÖŖ![]() ŗĶ
ŗĶ![]() Ėłŗ¬µÄŌ×ÓøöŹżĻąµČ£¬·Ö×ÓŹżÖ®±ČĪŖ
Ėłŗ¬µÄŌ×ÓøöŹżĻąµČ£¬·Ö×ÓŹżÖ®±ČĪŖ![]() ”£
”£![]() ŗĶ
ŗĶ![]() µÄŌ×ÓŗĖÄŚÖŹ×ÓŹż¶¼µČÓŚÖŠ×ÓŹż£¬
µÄŌ×ÓŗĖÄŚÖŹ×ÓŹż¶¼µČÓŚÖŠ×ÓŹż£¬![]() Ō×Ó
Ō×Ó![]() ²ćµē×ÓŹżŹĒ
²ćµē×ÓŹżŹĒ![]() ²ćµÄ3±¶”£
²ćµÄ3±¶”£
£Ø1£©![]() ”¢
”¢![]() µÄŌŖĖŲ·ūŗÅ·Ö±šĪŖ_______”£
µÄŌŖĖŲ·ūŗÅ·Ö±šĪŖ_______”£
£Ø2£©![]() ÖŠµÄ
ÖŠµÄ![]() ÖµĪŖ_______”£
ÖµĪŖ_______”£
£Ø3£©![]() µÄÄÜ²ćŹżÄæĪŖ_______”£
µÄÄÜ²ćŹżÄæĪŖ_______”£
£Ø4£©![]() ”¢
”¢![]() ŠĪ³ÉµÄŅ»ÖÖĘųĢ¬»ÆŗĻĪļÓėĖ®·“Ó¦ÄÜÉś³ÉÓÉ
ŠĪ³ÉµÄŅ»ÖÖĘųĢ¬»ÆŗĻĪļÓėĖ®·“Ó¦ÄÜÉś³ÉÓÉ![]() ”¢
”¢![]() ŠĪ³ÉµÄĮķŅ»ÖÖĘųĢ¬»ÆŗĻĪļ£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ_______”£
ŠĪ³ÉµÄĮķŅ»ÖÖĘųĢ¬»ÆŗĻĪļ£¬Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ_______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒŅ»øö»Æѧ¹ż³ĢµÄŹ¾ŅāĶ¼£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
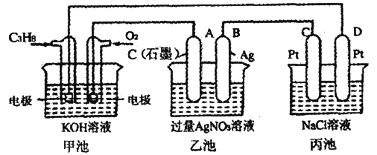
(1)¼×³ŲŹĒ___________×°ÖĆ£¬µē¼«BµÄĆū³ĘŹĒ___________”£
(2)¼××°ÖĆÖŠĶØČėC3H8µÄµē¼«·“Ó¦____________£¬±ū×°ÖĆÖŠD¼«µÄ²śĪļŹĒ___________(Š“»ÆѧŹ½)”£
(3)Ņ»¶ĪŹ±¼ä£¬µ±ŅŅ³ŲÖŠ²śÉś112 mL(±ź×¼×“æöĻĀ)ĘųĢåŹ±£¬¾łŌČ½Į°č±ū³Ų£¬ĖłµĆČÜŅŗŌŚ25”ꏱµÄpH=__________”£(ŅŃÖŖ£ŗNaClČÜŅŗ×ćĮ棬µē½āŗóČÜŅŗĢå»żĪŖ200 mL)”£
(4)ČōŅŖŹ¹ŅŅ³Ų»Öø“µē½āĒ°µÄדĢ¬£¬Ó¦ĻņŅŅ³ŲÖŠ¼ÓČė__________(Š“ĪļÖŹ»ÆѧŹ½)”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com