
【题目】某小组为探究三草酸合铁酸钾[K3[Fe(C2O4)3]·3H2O]的热分解产物,按下图所示装置进行实验。下列选项有关该实验的描述错误的是( )
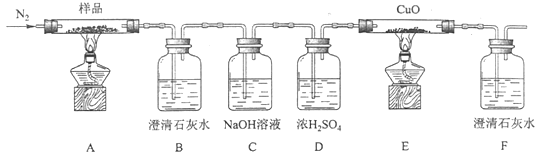
A.通入N2的目的是隔绝空气、使反应产生的气体全部进入到后续装置
B.装置E中现象若为黑色固体变红,F中澄清石灰水变浑浊,则证明分解产物中含有CO
C.停止实验时操作,应先熄灭装置A和E的酒精灯,再停止通入N2
D.结束实验后,待A中固体冷却至室温,取少量于试管中,加稀硫酸溶解,滴加1-2滴KSCN溶液,溶液变红,证明含有Fe2O3
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】一种芳纶纤维的拉伸强度比钢丝还高,广泛用作防护材料。其结构片段如下图
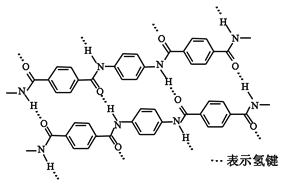
下列关于该高分子的说法正确的是
A. 完全水解产物的单个分子中,苯环上的氢原子具有不同的化学环境
B. 完全水解产物的单个分子中,含有官能团―COOH或―NH2
C. 氢键对该高分子的性能没有影响
D. 结构简式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NA是阿伏加德罗常数的值,下列说法错误的是
A.3g3He含有的中子数为NA
B.22gCO2与标准状况下11.2 L HF含有相同分子数
C.1 molK2Cr2O7被还原为Cr3+转移的电子数为6NA
D.在25℃、1.01×105 Pa的条件下,2.24LH2中含有的分子数小于0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A由C、H、O三种元素组成,在一定条件下,A、B、C、D、E之间的转变关系如图所示,请根据图示回答下列问题:

(1)C的官能团名称是___,D的结构简式为:___。
(2)图示反应中的①③反应类型分别属于___、___。
(3)下列说法不符合乙烯的是___(填写编号)。
a.乙烯在光照条件下易与氯气发生取代反应
b.乙烯分子中的所有原子处在同一平面上
c.可用燃烧法区分甲烷.乙烯和乙炔
(4)图示中反应①和③的化学方程为:___,___。
(5)A的同分异构体中(不包括A本身)与A属于同类物质的有___种,其中只有一个甲基的同分异构体的结构简式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知甲烷的燃烧热为890.3 kJ·mol-1,写出表示甲烷燃烧热的热化学方程式:__________________________
(2)如图是一个电化学过程的示意图,据图回答下列问题:
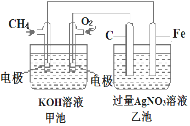
①甲池是___________________装置。
②请回答电极的名称:Fe电极的电极名称是__________
③写出电极反应式:通入CH4的电极反应式是__________________________;Fe电极的电极反应式为______________________
④乙池中反应的化学方程式为___________________________;当乙池中石墨(C)电极上生成的气体体积在标准状况下为112mL时,200mL AgNO3溶液(设乙池溶液的体积变化可以忽略)的pH值=_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯氧化铝可用于制高压钠灯的陶瓷管。实验室制取高纯氧化铝的流程如下:
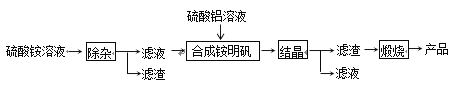
回答下列问题:
(1)硫酸铵溶液显酸性的原因是(用离子方程式表示)______________________________
(2)“除杂”操作是向硫酸铵溶液加入适量过氧化氢,再用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。该过程中,在酸性溶液条件下过氧化氢将Fe2+氧化成Fe3+的离子方程式为 _________________________,检验Fe2+已除尽的实验操作和现象是_______________________________
(3)通常条件下,若KSP[Fe(OH)3]=4.0×10-38,则理论上计算流程中“除杂”后溶液中c(Fe3+)等于____________mol·L-1
(4)配制硫酸铝溶液时,需用硫酸酸化,目的是__________________________________
(5)“结晶”操作中,母液经蒸发浓缩至溶液表面刚出现薄层的结晶为止,冷却结晶,得到铵明矾晶体(NH4Al(SO4)2·12H2O);该操作过程中,母液不能蒸干的原因是_________________________
(6)向铵明矾溶液中滴加极少量NaOH溶液时,反应的离子方程式是___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳和硅及其化合物的开发由来已久,在现代生活中有广泛应用。
(1)高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上制备高纯硅通常第一步是利用石英砂和焦炭在电弧炉中制粗硅,则该反应的化学方程式是______。
(2)某同学为了验证碳和硅两种元素非金属性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验),实验操作步骤:
步骤Ⅰ:打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加浓盐酸。
步骤Ⅱ:A中看到白色沉淀时,关闭弹簧夹1,打开弹簧夹2,关闭活塞a。

①通过步骤Ⅰ知浓盐酸具有的性质是_________(填字母)。
A.挥发性 B.还原性 C.氧化性 D.酸性
②C装置中的试剂X是_______(填化学式),D中试剂瓶的现象是___。
③该同学用图中所示装置进行实验验证碳和硅两种元素非金属性的相对强弱的理论依据是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上合成CH3OH的原理为:2H2(g)+CO![]() CH3OH(g),一定温度下,向1L恒容密闭容器中充入H2和CO,反应达平衡时CH3OH的体积分数与反应物投料之比(n(H2)/n(CO))的关系如图所示。下列说法错误的是
CH3OH(g),一定温度下,向1L恒容密闭容器中充入H2和CO,反应达平衡时CH3OH的体积分数与反应物投料之比(n(H2)/n(CO))的关系如图所示。下列说法错误的是
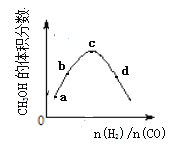
A. 相同条件下,达到平衡时混合气体的密度与反应前相同
B. a、b、c、d四点中,c点CO的转化率最大。
C. 若投料时n(CO)不变,a、b、c、d四点中d处CH3OH的物质的量最大
D. 图像中 c点到d点,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究锌与稀硫酸的反应速率(以v(H2)表示),向反应混合液中加入少量下列物质,下列判断正确的是
A. 加入NH4HSO4固体,v(H2)不变 B. 加入KNO3固体,v(H2)不变
C. 加入CH3COONa固体,v(H2)减小 D. 滴加CuSO4溶液,v(H2)减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com