
| A. | 反应物分子的每次碰撞都能发生化学反应 | |
| B. | 活化分子之间的碰撞一定是有效碰撞 | |
| C. | 能够发生化学反应的碰撞是有效碰撞 | |
| D. | 增大反应物浓度时,活化分子百分数增大 |
分析 活化分子之间的碰撞不一定为有效碰撞,当发生化学反应的碰撞才是有效碰撞,增大反应物浓度,活化分子的浓度增大,但百分数不变,以此解答该题.
解答 解:A.反应物分子的每次碰撞不一定为有效碰撞,则不一定发生化学反应,分子需达到足量的能量及合适的取向才反应,故A错误;
B.活化分子碰撞不一定发生反应,还与取向有关,则不一定为有效碰撞,故B错误;
C.能够发生化学反应的碰撞是有效碰撞,有效碰撞的条件:①活化分子,②有合适的取向,所以只有活化分子的有效碰撞才能发生化学反应,故C正确;
D.增大反应物浓度时,增大单位体积内活化分子个数,但活化分子百分数不变,故D错误;
故选C.
点评 本题考查影响化学反应速率的因素,明确温度、压强、催化剂、浓度等对反应的影响即可解答,注意碰撞理论的理解为解答的难点,题目难度中等.


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:填空题

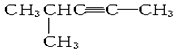 分子式为C5H8,名称是4-甲基-1-戊炔,
分子式为C5H8,名称是4-甲基-1-戊炔,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中加入稀氨水,水的电离平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 | |
| C. | 向水中加入少量CH3COOH,水的电离平衡逆向移动,c(H+)降低 | |
| D. | 将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④②⑤③ | B. | ④①②⑤③ | C. | ④②⑤①③ | D. | ⑤②④①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18 g H2O中含有2 mol氢 | |
| B. | 阿伏加德罗常数是指0.012 kg碳所含有的碳原子数,其数值约等于6.02×1023 | |
| C. | 铁的摩尔质量及其相对原子质量均为56 g•mol-1 | |
| D. | 常温常压下,44 g CO2气体与46 g N2O4气体具有相同数目的氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8种 | B. | 12种 | C. | 16种 | D. | 18种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率是对可逆反应而言的,非可逆反应不谈化学反应速率 | |
| B. | 在可逆反应中,正反应的化学反应速率是正值,逆反应的化学反应速率是负值 | |
| C. | 同一化学反应中,化学反应速率可用反应物浓度的改变表示,也可用生成物浓度的改变表示,其值可能相同,也可能不同 | |
| D. | 化学反应速率的单位可以是g/(L•s),也可以是kg/(L•s) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com