
【题目】下列各组溶液同时开始反应,最先出现浑浊现象的是( )
组 别 | 反应 温度 (℃) | 反应物 | 加水 体积 (ml) | |||
Na2S2O3 | H2SO4 | |||||
体积 (ml) | 浓度 (mol/L) | 体积 (ml) | 浓度 (mol/L) | |||
A | 40 | 5 | 0.2 | 5 | 0.1 | 10 |
B | 10 | 10 | 0.1 | 10 | 0.1 | 0 |
C | 10 | 5 | 0.1 | 5 | 0.2 | 10 |
D | 40 | 5 | 0.2 | 5 | 0.2 | 10 |
A. A B. B C. C D. D
 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示: 
(1)该反应的化学方程式为 .
(2)从反应开始到10s时,用Y表示的反应速率为 , X的转化率为 . (保留三位有效数字)
(3)10s时,该反应达到了化学平衡状态.(填“是”或“否”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把 0.6molX气体和0.4molY气体混合于2L的密闭容器中,使它们发生如下反应 3X(g)+Y(g)nZ(g)+2W(g),5min末已生成 0.2molW,若测知以 Z 表示的平均反应速率为 0.01molL﹣1min﹣1 , 则 n是( )
A.2
B.4
C.1
D.3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中反应制得:①3SiO2+6C+2N2![]() Si3N4+6CO;也可由SiCl4的蒸汽和NH3反应制取:②3SiCl4+4NH3
Si3N4+6CO;也可由SiCl4的蒸汽和NH3反应制取:②3SiCl4+4NH3![]() Si3N4+12HCl。则下列叙述正确的是
Si3N4+12HCl。则下列叙述正确的是
A. 反应②属于离子反应
B. 若制取等量的Si3N4,则反应①②转移电子数目必然相等
C. 反应①的氧化剂是N2
D. 反应①中氧化产物与还原产物物质的量之比为1∶6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲烷的电子式为 , 碳氢键之间键角为 . 甲烷和氯气在光照下发生取代反应,生成种产物.产物中常用作灭火剂.试写出三溴甲烷在光照条件下与溴蒸气反应的化学方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应2NO2(g)![]() N2O4(g)达到平衡后,在温度不变时欲使c(NO2)/c(N2O4)比值增大,可以采取的措施是
N2O4(g)达到平衡后,在温度不变时欲使c(NO2)/c(N2O4)比值增大,可以采取的措施是
A. 体积不变,增加NO2的量 B. 体积不变,增加N2O4的量
C. 体积不变,充入N2 D. 体积扩大到原来的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:
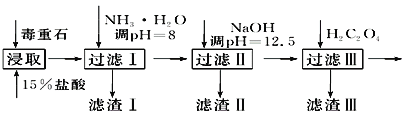
(1)毒重石用盐酸浸取前需充分研磨,目的是_______________________________________;实验室用37%的盐酸配制15%的盐酸,除量筒外还需使用下列仪器中的________。
a.烧杯 b.一定容积的容量瓶 c.玻璃棒 d.滴定管
(2)查阅有关资料获得沉淀各种杂质离子的pH见下表:
沉淀杂质离子 | Ca2+ | Mg2+ | Fe3+ |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
加入NH3·H2O调节pH=8可除去______(填离子符号);滤渣Ⅱ中含__________(填化学式)。加入H2C2O4时应避免过量,原因是_____________________(已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9)。
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。已知:2CrO![]() +2H+===Cr2O
+2H+===Cr2O![]() +H2O Ba2++CrO
+H2O Ba2++CrO![]() ===BaCrO4↓
===BaCrO4↓
步骤Ⅰ.准确移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入几滴酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0 mL。
步骤Ⅱ.准确移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ 相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。
滴加盐酸标准液时应用酸式滴定管,“0”刻度位于滴定管的________(选填“上方”或“下方”)。BaCl2溶液的浓度为________________mol·L-1,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,则所测得Ba2+浓度测量值将________(选填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验原理或操作正确的是( )
A. 用20mL量筒量取15mL酒精,加水5mL,配制质量分数为75%的酒精溶液(P<1)
B. 在200mL某硫酸盐溶液中,含有1.5NA个硫酸根离子,同时含有NA个金属离子,则该硫酸盐的物质的量浓度为2.5mol·L-1
C. 实验中需用2.0mol·L-1的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分数分别为950mL、201.4g
D. 实验室配制500mL 0.2mol·L-1的硫酸亚铁溶液,其操作是:用天平称15.2g绿矾(FeSO47H2O),放入小烧杯中加水溶解,转移到500mL容量瓶、稀释、定量、摇匀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com