
【题目】用下列实验装置进行相应实验,能达到实验目的的是( )
A.用图1所示装置除去Cl2中含有的少量HCl
B.用图2所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图3所示装置制取少量纯净的CO2气体
D.用图4所示装置分离CCl4萃取碘水后已分层的有机层和水层
【答案】D
【解析】
A.氯气、HCl均与NaOH溶液反应,不能除杂,应选饱和食盐水除去Cl2中含有的少量HCl,故A不符合题意;
B.蒸干NH4Cl饱和溶液,氯化铵分解,应蒸发浓缩、冷却结晶法制备NH4Cl晶体,故B不符合题意;
C.纯碱为粉末固体,关闭止水夹不能使固体与液体分离,且碳酸钠易溶于水,则不能制取少量纯净的CO2气体,故C不符合题意;
D.碘易溶于四氯化碳,与水分层后有机层在下层,则装置可分离CCl4萃取碘水后已分层的有机层和水层,故D符合题意;
答案为D
A.除杂只能选择仅和杂质反应的试剂:氯气、HCl均与NaOH溶液反应
B.蒸发结晶只适合受热稳定的固体:氯化铵受热分解(需采取降温结晶)
C.碳酸钠易溶于水,不适合固体与液体分离装置,需换成石灰石;且CO2气体中含水
D.萃取分液需选择仪器为分液漏斗,溶剂要求不溶于水


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某酸性废液中含有Fe2+、Cu2+、Ba2+三种金属离子,有同学设计了下列方案对废液进行处理(所加试剂均稍过量),以回收金属,保护环境。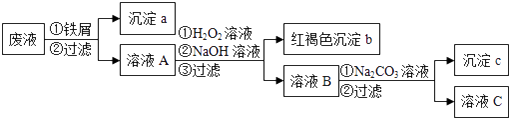
请回答:
(1)沉淀a中含有的单质是;
(2)沉淀b的化学式是;
(3)沉淀c的化学式是;
(4)溶液A与H2O2溶液在酸性条件下反应的离子方程式是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(H2O2),当它们混合时,即产生大量的N2和水蒸气,并放出大量热.已知0.4mol液态肼和足量H2O2反应,生成氮气和水蒸气,放出256.65kJ的热量.
(1)写出该反应的热化学方程式: .
(2)已知H2O(l)═H2O(g);△H=+44kJmol﹣1,则16g液态肼燃烧生成氮气和液态水时,放出的热量是kJ.
(3)上述反应应用于火箭推进剂,除释放大量的热和快速产生大量气体外,还有一个很突出的优点是 .
(4)已知N2(g)+2O2(g)═2NO2(g);△H=+67.7kJmol﹣1,N2H4(g)+O2(g)═N2(g)+2H2O (g);△H=﹣534kJmol﹣1,根据盖斯定律写出肼与NO2完全反应生成氮气和气态水的热化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方法能达到实验目的是( )
A.用分液漏斗从食醋中分离出乙酸
B.用焰色反应鉴别Na2SO4和Na2CO3
C.用NaOH溶液除去Cl2中含有的少量HCl
D.用KSCN溶液检验FeCl3溶液 中是否含有Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列仪器中①漏斗;②容量瓶;③蒸馏烧瓶;④天平;⑤分液漏斗;⑥燃烧匙,常用于物质分离的是 ( )
A. ①③④ B. ①②⑥ C. ①③⑤ D. ③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①镧系合金是稀土系储氢合金的典型代表,由荷兰菲利浦实验室首先研制出来。它的最大优点是容易活化,其晶胞结构如图所示。 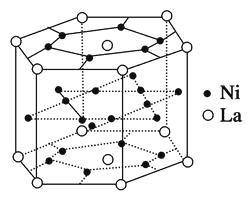
它的化学式为。
②镁系合金是最早问世的合金之一,经X射线衍射实验分析得镁铜合金为面心立方结构,镁镍合金为六方最密堆积。镁系合金的优点是价格较低,缺点是要加热到250℃以上时才释放出氢气。下列有关说法不正确的是
A.金属铜的晶胞结构为 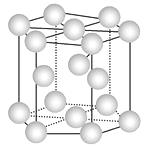
B.已知钛和镁的堆积方式相同,均为六方最密堆积,则其堆积方式为 
C.镁铜合金晶体的原子空间利用率为74%
D.镁镍合金晶体的配位数为12
③《X射线金相学》中记载关于铜与金可形成两种有序的金属互化物,其结构如图。下列有关说法正确的是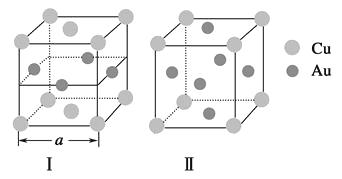
A.图Ⅰ、Ⅱ中物质的化学式相同
B.图Ⅱ中物质的化学式为CuAu3
C.图Ⅱ中与每个铜原子紧邻的铜原子有3个
D.设图Ⅰ中晶胞的边长为acm,则图Ⅰ中合金的密度为 ![]() g·cm-3
g·cm-3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学反应的本质的说法正确的是( )
A.化学反应都有新物质生成
B.化学反应都有能量变化
C.化学反应是旧键断裂新键形成的过程
D.化学反应的发生都需要在一定条件下
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有原子序数小于20的A、B、C、D、E、F6种元素,它们的原子序数依次增大,已知B元素是地壳中含量最多的元素;A和C的价电子数相同,B和D的价电子数也相同,且A和C两元素原子核外电子数之和是B、D两元素原子核内质子数之和的;C、D、E三种元素的基态原子具有相同的电子层数,且E原子的p轨道上电子数比D原子的p轨道上多一个电子;6种元素的基态原子中,F原子的电子层数最多且和A处于同一主族。回答下列问题:
(1)用电子式表示C和E形成化合物的过程。
(2)写出基态F原子的核外电子排布式。
(3)写出A2D的电子式 , 其分子中(填“含”或“不含”,下同)σ键,π键。
(4)A、B、C共同形成的化合物中化学键的类型有。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com