
| A、将过量的NaOH溶液滴入同浓度的少量Ca(HCO3)2溶液中Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
| B、向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全Ba2++OH-+H++SO42-=BaSO4↓+H2O |
C、服用阿司匹林过量出现水杨酸( )反应,可静脉注射碳酸氢钠溶液: )反应,可静脉注射碳酸氢钠溶液: |
| D、向FeI2溶液中加少量氯水 2Fe2++Cl2=2Fe3++2Cl- |
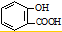 +HCO3-=H2O+CO2↑+
+HCO3-=H2O+CO2↑+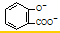 ,故C错误;
,故C错误;

科目:高中化学 来源: 题型:
| 主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
| B、硫酸钠与氯化钡溶液混和:SO42-+Ba2+═BaSO4↓ |
| C、硝酸滴在石灰石上:CaCO3+2H+═Ca2++H2CO3 |
| D、氧化铜与硫酸混和:Cu2++SO42-═CuSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜加入稀硝酸中:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O | ||||
| B、铁粉溶于稀盐酸中:2Fe+6H+=2Fe3++3H2↑ | ||||
| C、碳酸钙和盐酸反应:CO32-+2H+=CO2↑+H2O | ||||
D、实验室用浓盐酸与MnO2反应制Cl2:MnO2+2H++2Cl-
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验内容 |  |
 |
 |
 |
| 实验目的 | 实验室制备氨气 | 测定盐酸浓度 | 配制稀硫酸溶液 | 氯化氢尾气吸收 |
| A | B | C | D |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①中有:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| B、②中有:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
| C、①和②混合溶液中:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
| D、①或②中都有:c(HCO3-)+c(CO32-)+c(H2CO3)=0.10 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向含Pb2+、Cu2+、Hg2+的浓度均为0.010 mol?L-1的溶液中通人硫化氢气体,产生沉淀的顺序依次为PbS、CuS、HgS |
| B、在硫化铅悬浊液中滴几滴硝酸铜溶液,会生成硫化铜 |
| C、在含Hg2+、Cu2+、Pb2+的溶液中滴加硫化钠溶液,当c(S2-)=0.001 mol?L-1时三种金属离子都完全沉淀 |
| D、硫化钠是处理废水中含上述金属离子的沉淀剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、Zn电极上发生还原反应 |
| B、片刻后盐桥中的Cl-向乙装置中移动 |
| C、片刻后在a点滴加酚酞观察到滤纸变红色 |
| D、片刻后在b点滴加淀粉碘化钾溶液观察到滤纸无变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com