
下列离子方程式不正确的是( )
A.NH4HCO3溶于过量的浓KOH溶液中:NH4+ + HCO3-+ 2OH- = CO32- + NH3↑+ 2H2O
B.双氧水中加入稀硫酸和KI溶液:H2O2 + 2H+ + 2I— = I2 + 2H2O
C.向FeBr2溶液中通入足量氯气:2Fe2+ + 4Br- + 3Cl2 = 2Fe3+ + 2Br2 + 6Cl-
D.Na2S 2O3溶液中加入稀硫酸:2S2O32—+ 4H+ =SO42— + 3S↓ + 2H2O
2O3溶液中加入稀硫酸:2S2O32—+ 4H+ =SO42— + 3S↓ + 2H2O
科目:高中化学 来源:2016届北京市高三上学期期中测试化学试卷(解析版) 题型:选择题
高铁酸钾(K2FeO4)是一种既能杀菌消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式为Fe(OH)3+ClO-+OH-→FeO+Cl-+H2O(未配平),下列有关说法不正确的是
A.由上述反应可知,Fe(OH)3的氧化性强于FeO
B.高铁酸钾中铁显+6价
C.上述反应中氧化剂和还原剂的物质的量之比为3∶2
D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省高一上学期期中测试化学试卷(解析版) 题型:选择题
下列对于某些离子的检验及结论正确的是
A、某溶液加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,则一定含有CO32一
B、某溶液加入氢氧化钠溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝,则一定含有NH4+
C、某溶液滴入BaCl2溶液,再滴加稀盐酸,产生白色沉淀,则一定含有SO42一
D、某溶液加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,则一定含有Ba2+
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三11月月考化学试卷(解析版) 题型:选择题
饱和氯水中存在如下平衡:①Cl2+H2O H++Cl-+HClO ;②HClO
H++Cl-+HClO ;②HClO H++ClO-,将饱和氯水倒入试管中分别进行下列实验,相应分析结论错误的是( )
H++ClO-,将饱和氯水倒入试管中分别进行下列实验,相应分析结论错误的是( )
A.加入CaCO3悬浊液,CaCO3的溶解平衡向右移动
B.加入澄清石灰水,c(H+)一定减小
C.加入一定量NaOH溶液后,溶液中离子浓度的关系可能为c(Cl-) +c(ClO-) =c(Na+)
D.通入过量Cl2,①、②均向右移动,溶液pH减小
查看答案和解析>>
科目:高中化学 来源:2016届宁夏育才中学高三上学期第四次月考化学试卷(解析版) 题型:填空题
某种食用精制盐包装袋上有如下说明:
产品标准 | GB5461 |
产品等级 | 一级 |
配 料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50mg/kg |
分装时期 | |
分装企业 |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处) KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是 。
②某学生设计回收四氯化碳的操作为:
A.将碘的四氯化碳溶液置于分液漏斗中;
B.加入适量Na2SO3稀溶液;
C.分离出下层液体;
D.将分液漏斗充分振荡后静置
其中分液漏斗使用前须进行的操作是 ,上述操作正确的顺序是: (填序号)
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
A.准确称取wg食盐,加适量蒸馏水使其完全溶解;
B.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
C.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液10.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是 。
②b中反应所产生的I2的物质的量是 mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示) mg/kg。
查看答案和解析>>
科目:高中化学 来源:2016届湖北武汉华中师大一附中等八校高三上联考一理化学卷解析版 题型:填空题
E、G、M、Q、T是五种原子序数依次增大的前四周期元素。E、G、M是位于P区的同一周期的元素,M的价层电子排布为nsnnp2n,E与M原子核外的未成对电子数相等;QM2与GM2-为等电子体;T为过渡元素,其原子核外没有未成对电子。请回答下列问题:
(1)与T同区、同周期元素原子价电子 排布式是 。
排布式是 。
(2)E、G、M均可与氢元素形成氢化物,它们的最简单氢化物在固态时都形成分子晶体,其中晶胞结构与干冰不一样的是 (填分子式)。
(3)E、G、M的最简单氢化物中,键角由大到小的顺序为 (用分子式表示),其中G的最简单氢化物的VSEPR模型名称为 ,M的最简单氢化物的分子立体构型名称为 。
(4)EM、GM+、G2互为等电子体,EM的结构式为(若有配位键,请用“→”表示) 。E、M电负性相差1.0,由此可以判断EM应该为极性较强的分子,但实际上EM分子的极性极弱,请解释其原因 。
(5)TQ在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方TQ晶体结构如图所示,该晶体的密度为ρ g·cm-3。如果TQ的摩尔质量为M g/mol,阿伏加德罗常数为NA mol-1,则a、b之间的距离为 cm。
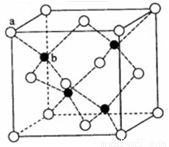
查看答案和解析>>
科目:高中化学 来源:2016届海南省等七校联盟高三第一次联考化学卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列叙述正确的是
A.0.1mol·L-1的NaCl溶液中Cl-的数目为0.1NA
B.16g O3中所含的氧原子数为NA
C.22.4L H2中含有的氢原子数一定为2NA
D.1molCl2与过量的金属钠充分反应后,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西大学附属中学高一上期中化学试卷(解析版) 题型:填空题
在实验室里,某同学做金属钠与水反应等实验。试完成下列问题:
(1)在空气中把金属钠切开并观察切面,很快就看到的现象是_________________,所发生反应的化学方程式是________________________。
(2)将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是①______________________,②____________________________。
钠与水反应的离子方程式为___________________________。在反应过程中,若生成标准状况下224 mL的H2,则转移电子的数目为_________。
(3)将一小块钠投入盛有饱和石灰水的烧杯中,不可能观察到的现象是________。
A.能听到“嘶嘶”的响声 B.钠熔化成小球并在液面上游动
C.溶液变浑浊 D.烧杯底部有银白色的金属钙生成
(4)根据上述实验过程中钠所发生的有关变化,试说明将金属钠保存在煤油中的目的是______________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江余姚中学高二上学期期中考试化学试卷(解析版) 题型:选择题
今有室温下四种溶液,下列叙述不正确的是
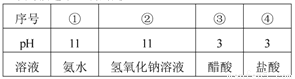
A.③④中分别加入适最的醋酸钠晶体后,两溶液的pH均增大
B.②③两溶液等体积混合.所得溶液中c(H+)>c(OH-)
C.分别加水稀释10倍.四种溶液的pH值大小关系为:①>②>④>③
D.V1L④与V2L①溶液混合后,若混合后溶液pH=7.则V1<V2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com