

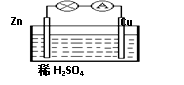
| A.负极的反应式为2H++2e-==H2↑ |
| B.电流由Zn经外电路流向Cu |
| C.反应一段时间后,溶液中的c(H+)减小 |
| D.溶液中H+向负极移动 |
科目:高中化学 来源:不详 题型:填空题

| A.金属活动性铝比镁强 |
| B.金属活动性镁比铝强,两装置中镁均为负极 |
| C.仅根据金属活动性顺序不能准确判断原电池的正负极 |
| D.原电池中的正负极受电解质溶液的酸碱性、强氧化性等因素的影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.b>a>c | B.a>b>c | C.c>b>a | D.c>a>b |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
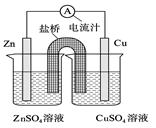
| A.Cu电极为正电极 |
| B.原电池工作时,电子从Zn电极流出 |
| C.原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu |
| D.盐桥(琼脂-饱和KCl溶液)中的K+移向ZnSO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.①②③ |
| C.②③④ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
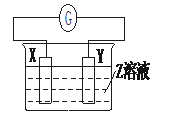
| 编号 | X | Y | Z |
| A | Zn | Cu | 稀硫酸 |
| B | Cu | Zn | 稀硫酸 |
| C | Cu | Ag | 硫酸铜溶液 |
| D | Ag | Zn | 硝酸银溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
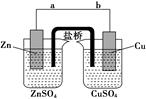
| A.盐桥中的K+移向ZnSO4溶液 |
| B.电池总反应为:Zn+Cu2+==Zn2++Cu |
| C.在外电路中,电子从负极流向正极 |
| D.负极反应为:Zn-2e-==Zn2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com