
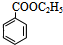 ,E
,E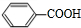 .
.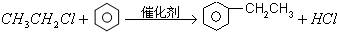 ;②CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O;⑥
;②CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O;⑥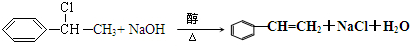 .H→I
.H→I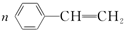 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ .
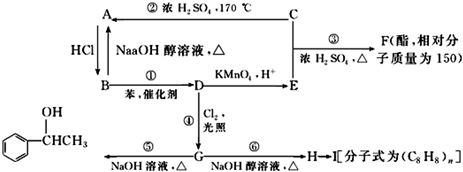
. 分析 A是水果的催熟剂,A为CH2=CH2;C是生活中常见的有机物,能发生反应生成A,结合反应条件知,C为CH3CH2OH,A和HCl发生加成反应生成B,B能发生消去反应生成A,则B为CH3CH2Cl,B发生反应生成D,D发生一系列反应生成I,H发生加聚反应生成H,则D和H中碳原子个数都是8,B发生取代反应生成D,则D为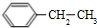 ,D发生氧化反应生成E为
,D发生氧化反应生成E为 ,C和E发生酯化反应生成F,根据F相对分子质量知,F结构简式为
,C和E发生酯化反应生成F,根据F相对分子质量知,F结构简式为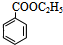 ;
;
D发生取代反应生成G,G发生取代反应生成 ,故G为
,故G为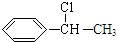 ,G发生消去反应生成H为
,G发生消去反应生成H为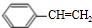 ,H发生加聚反应生成高聚物I为
,H发生加聚反应生成高聚物I为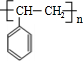 ,据此分析解答.
,据此分析解答.
解答 解:A是水果的催熟剂,A为CH2=CH2;C是生活中常见的有机物,能发生反应生成A,结合反应条件知,C为CH3CH2OH,A和HCl发生加成反应生成B,B能发生消去反应生成A,则B为CH3CH2Cl,B发生反应生成D,D发生一系列反应生成I,H发生加聚反应生成H,则D和H中碳原子个数都是8,B发生取代反应生成D,则D为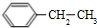 ,D发生氧化反应生成E为
,D发生氧化反应生成E为 ,C和E发生酯化反应生成F,根据F相对分子质量知,F结构简式为
,C和E发生酯化反应生成F,根据F相对分子质量知,F结构简式为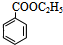 ;
;
D发生取代反应生成G,G发生取代反应生成 ,故G为
,故G为 ,G发生消去反应生成H为
,G发生消去反应生成H为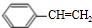 ,H发生加聚反应生成高聚物I为
,H发生加聚反应生成高聚物I为 ,
,
(1)通过以上分析知,A、F、E的结构简式分别为CH2=CH2、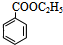 、
、 ,
,
故答案为:CH2=CH2;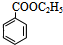 ;
; ;
;
(2)在①~⑥6个反应中,属于消去反应的是②⑥,
故答案为:②⑥;
(3)①为氯乙烷和苯的取代反应,反应方程式为: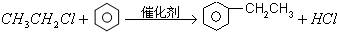 ;
;
②为乙醇的消去反应,反应方程式为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O;
⑥反应方程式为 ;
;
H→I反应方程式为: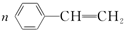 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ ,
,
故答案为: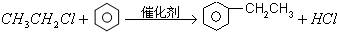 ;CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O;
;CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O; ;
;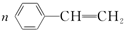 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ .
.
点评 本题考查有机物推断,为高频考点,题目难度中等,侧重考查学生分析推断能力,明确物质中官能团及其性质关系、反应条件及反应特点是解本题关键.


科目:高中化学 来源: 题型:选择题
| A. | 通过石灰水 | |
| B. | 通过品红溶液 | |
| C. | 先通过小苏打溶液,再通过石灰水 | |
| D. | 先通过足量溴水溶液,再通过石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
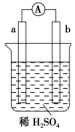 在如图所示的装置中,a的金属活泼性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )
在如图所示的装置中,a的金属活泼性比氢要强,b为碳棒,关于此装置的各种叙述不正确的是( )| A. | 碳棒上有气体放出,溶液c(H+)减小 | |
| B. | a是正极,b是负极 | |
| C. | 导线中有电子流动,电子从a极到b极 | |
| D. | a极上发生了氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.2 LNH3所含分子数为0.5NA | |
| B. | 1molCl2与足量Fe反应,转移的电子数为3NA | |
| C. | 23g金属钠与氧气加热生成Na2O2的反应,转移的电子数为2NA | |
| D. | 5.6g铁与足量的盐酸反应,失去的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 中和反应中,反应物的总能量比生成物的总能量低 | |
| B. | 化学反应中能量变化的主要原因是化学键的断裂与生成 | |
| C. | 图I所示的装置能将化学能转变为电能 | |
| D. | 图Ⅱ所示的反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
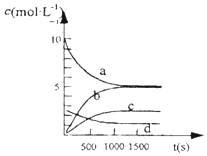 (1)已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ/mol
(1)已知:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ/mol| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(ml) | 20 | 13.96 | 10.08 | 10.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 缓慢通入N2,再加热Ⅰ处的碳酸氢钠,可观察到Ⅱ处过氧化钠粉末由浅黄色变成白色 | |
| B. | 缓慢通入N2,加热Ⅰ处KClO3和MnO2的混合物,可观察到Ⅱ处干燥KI淀粉试纸变成蓝色 | |
| C. | 先对Ⅰ处的氯化铵加热,再缓慢通入N2,可看到Ⅰ处固体减少,Ⅱ处无固体沉积 | |
| D. | 先缓慢通入CO2,再加热Ⅰ处炭粉,可观察到Ⅱ处氧化铁粉末由红色变成黑色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溴水鉴别乙烯和CO2 | |
| B. | 用pH试纸鉴别NaCl溶液与Na2CO3溶液 | |
| C. | 用观察外观颜色的方法区别氧化铁和氧化铜 | |
| D. | 用石灰水鉴别CO2和SO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com