

| æŖŹ¼³ĮµķµÄpH | ³ĮµķĶźČ«µÄpH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
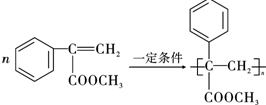
·ÖĪö £Ø1£©ĖįŠŌĢõ¼žĻĀCuÓė¹żŃõ»ÆĒā·¢ÉśŃõ»Æ»¹Ō·“Ӧɜ³ÉĮņĖįĶŗĶĖ®£»¹żŃõ»ÆĒā¼ÓČȵ½153”ę±ćĆĶĮŅµÄ·Ö½ā£»
£Ø2£©¢Łøł¾Żµķ·ŪÓėµāµ„ÖŹ×÷ÓƱ䥶½ā“š£»
¢Śøł¾ŻH2O2+2I-+2H+=I2+2H2O½ā“š£»
¢Ūøł¾Ż·“Ó¦2Cu2++4I-ØT2CuI£Ø°×É«£©”ż+I2 ŗĶ2S2O32-+I2ØT2I-+S4O62-£¬ÓŠ¹ŲĻµŹ½Cu2+”«S2O32-£¬øł¾ŻNa2S2O3µÄĪļÖŹµÄĮææɼĘĖćµĆCu2+µÄĪļÖŹµÄĮ棬½ų¶ųČ·¶ØCu2+ĪļÖŹµÄĮæÅØ¶Č£»
£Ø3£©µĪ¼ÓH2O2ČÜŅŗ£¬Ź¹Fe2+×Ŗ»ÆĶźČ«ĪŖFe3+£¬µĪ¼ÓNaOHČÜŅŗ£¬ŠĪ³ÉĒāŃõ»ÆĢś³Įµķ£¬³żŌÓŗóŠĪ³ÉĒāŃõ»ÆŠæ³Įµķ£¬¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ900”ęģŃÉÕÖʵĆŃõ»ÆŠæ£®
½ā“š ½ā£ŗ£Ø1£©ŅņĪŖĖ«ŃõĖ®ŌŚĖįŠŌČÜŅŗÖŠĻČ°ŃĶŃõ»Æ³ÉŃõ»ÆĶ£¬µ±Č»ÕāŹĒŅ»øöĪ¢ČõµÄ·“Ó¦£¬ŠĪ³ÉŅ»øöĘ½ŗā£¬µ«ŹĒŠĪ³ÉµÄŃõ»ÆĶĀķÉĻ¾Ķ»į±»Ļ”ĮņĖįČܽā£¬Ę½ŗā±»“ņĘĘ£¬·“Ó¦³ÆÕż·½Ļņ½ųŠŠ£¬¹Ź¶ųÖš½„Čܽā£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCu+H2O2+H2SO4=CuSO4+2H2O£¬¹żŃõ»ÆĒāŠŌÖŹ±Č½ĻĪČ¶Ø£¬Čō¼ÓČȵ½153”ę±ćĆĶĮŅµÄ·Ö½āĪŖĖ®ŗĶŃõĘų£¬½«ČÜŅŗÖŠ¹żĮæµÄH2O2 ³żČ„æɼÓČČÖĮ·Š£¬
¹Ź“š°øĪŖ£ŗCu+H2O2+H2SO4=CuSO4+2H2O£»¼ÓČČÖĮ·Š£»
£Ø2£©¢Łøł¾Żµķ·ŪÓėµāµ„ÖŹ×÷ÓƱ䥶æÉÖŖ£¬æÉÓƵķ·ŪČÜŅŗĪŖÖøŹ¾¼Į£¬
¹Ź“š°øĪŖ£ŗµķ·ŪČÜŅŗ£»
¢ŚČōĮōÓŠH2O2£¬¼ÓČėKIŗ󣬻įÓŠŅŌĻĀ·“Ó¦£ŗH2O2+2I-+2H+=I2+2H2OĪóµ±³É2Cu2++4I-=2CuI£Ø°×É«£©”ż+I2 Éś³ÉµÄµā£¬Ź¹²ā¶Ø½į¹ūĘ«øߣ¬
¹Ź“š°øĪŖ£ŗĘ«øߣ»
¢Ūøł¾Ż·“Ó¦2Cu2++4I-ØT2CuI£Ø°×É«£©”ż+I2 ŗĶ2S2O32-+I2ØT2I-+S4O62-£¬ÓŠ¹ŲĻµŹ½Cu2+”«S2O32-£¬øł¾ŻĢāŅāæÉÖŖNa2S2O3µÄĪļÖŹµÄĮæĪŖ0.1mol/L”Į0.025L=0.0025mol£¬ĖłŅŌČÜŅŗÖŠCu2+µÄĪļÖŹµÄĮæĪŖ0.0025mol£¬²āČÜŅŗÖŠCu2+ĪļÖŹµÄĮæÅضČĪŖ$\frac{0.0025mol}{0.02L}$=0.125mol/L£¬
¹Ź“š°øĪŖ£ŗ0.125mol/L£»
£Ø3£©¢ŁĻņĀĖŅŗÖŠ¼ÓČė30%H2O2£¬Ź¹Ęä³ä·Ö·“Ó¦£¬ÄæµÄŹ¹Fe2+×Ŗ»ÆĶźČ«ĪŖFe3+£¬µĪ¼ÓNaOHČÜŅŗ£¬µ÷½ŚČÜŅŗPHŌ¼ĪŖ5£Ø»ņ3.2”ÜpH£¼5.9£©£¬Ź¹Fe3+³ĮµķĶźČ«£¬ĻņĀĖŅŗÖŠµĪ¼Ó1.0mol•L-1NaOH£¬µ÷½ŚČÜŅŗPHŌ¼ĪŖ10£Ø»ņ8.9”ÜpH”Ü11£©£¬Ź¹Zn2+³ĮµķĶźČ«£¬900”ęģŃÉÕ£¬ÖʵĆŃõ»ÆŠæ£¬
¹Ź“š°øĪŖ£ŗĻņĀĖŅŗÖŠ¼ÓČė30%H2O2£¬Ź¹Ęä³ä·Ö·“Ó¦£»µĪ¼Ó1.0mol•L-1NaOH£¬µ÷½ŚČÜŅŗPHŌ¼ĪŖ5£Ø»ņ3.2”ÜpH£¼5.9£©£¬Ź¹Fe3+³ĮµķĶźČ«£»ĻņĀĖŅŗÖŠµĪ¼Ó1.0mol•L-1NaOH£¬µ÷½ŚČÜŅŗPHŌ¼ĪŖ10£Ø»ņ8.9”ÜpH”Ü11£©£¬Ź¹Zn2+³ĮµķĶźČ«£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éŹµŃéŹŅ·ĻĘś¾Éµē³ŲµÄĶƱ»ŲŹÕĶŗĶÖʱøZnO£¬æ¼²éѧɜ¶Ō×ŪŗĻŹµŃ铦ĄķÄÜĮ¦£¬×¢ŅāŹµŃé·½°øµÄÉč¼ĘŌĄķŗĶ²½ÖčŹĒ½ā“šµÄ¹Ų¼ü£¬Ę½Ź±×¢Ņā“ņŗĆŌśŹµµÄ»ł“”ÖŖŹ¶ŗĶĮé»īÓ¦ÓĆÖŖŹ¶½ā¾öĪŹĢāµÄÄÜĮ¦ÅąŃų£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
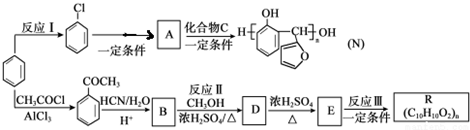
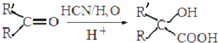
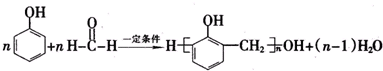
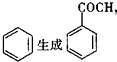 µÄ·“Ó¦ĄąŠĶŹĒČ”“ś·“Ó¦£¬DÉś³ÉEµÄ¹ż³ĢÖŠ£¬ÅØĮņĖįµÄ×÷ÓĆŹĒ“߻ƼĮŗĶĶŃĖ®¼Į•
µÄ·“Ó¦ĄąŠĶŹĒČ”“ś·“Ó¦£¬DÉś³ÉEµÄ¹ż³ĢÖŠ£¬ÅØĮņĖįµÄ×÷ÓĆŹĒ“߻ƼĮŗĶĶŃĖ®¼Į•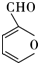
 £®
£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.025 mol | B£® | 0.050 mol | C£® | 0.100 mol | D£® | 0.200 mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ²ŻĖįÓėĖįŠŌøßĆĢĖį¼ŲČÜŅŗ·“Ó¦£ŗ2MnO4-+5H2C2O4+6H+ØT2Mn2++10CO2”ü+8H2O | |
| B£® | Įņ“śĮņĖįÄĘÓėĮņĖįµÄĄė×Ó·½³ĢŹ½£ŗS2O32-+2H+ØTSO2”ü+S”ż+H2O | |
| C£® | KIČÜŅŗÖŠµĪ¼ÓĻ”ĮņĖį£¬³ØæŚ·ÅÖĆ£ŗ2H++2I-+O2ØTI2+2H2O | |
| D£® | K2Cr2O7µÄČÜŅŗÖŠ“ęŌŚµÄĘ½ŗāĢåĻµ£ŗCr2O72-+H2O?2CrO42-+2H+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ę½ŗāĒ°£¬³äČėµŖĘų£¬ČŻĘ÷ÄŚŃ¹ĒæŌö“󣬷“Ó¦ĖŁĀŹ¼Óæģ | |
| B£® | Ę½ŗāŹ±£¬ĘäĖūĢõ¼ž²»±ä£¬·ÖĄė³öĮņ£¬Äę·“Ó¦ĖŁĀŹ¼õŠ” | |
| C£® | Ę½ŗāŹ±£¬ĘäĖūĢõ¼ž²»±ä£¬ÉżøßĪĀ¶ČæÉĢįøß SO2 µÄ×Ŗ»ÆĀŹ | |
| D£® | ĘäĖūĢõ¼ž²»±ä£¬ĖõŠ”ČŻĘ÷Ģå»ż£¬Ę½ŗāÕż·“Ó¦·½ĻņŅĘ¶Æ£¬øĆ·“Ó¦µÄĘ½ŗā³£Źż²»±ä |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
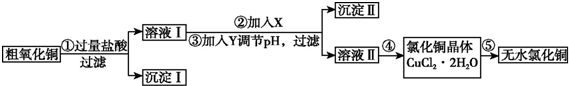
| ĒāŃõ»ÆĪļæŖŹ¼³ĮµķŹ±µÄpH | ĒāŃõ»ÆĪļ³ĮµķĶźČ«Ź±µÄpH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
| Ģį¹©µÄŹŌ¼Į£ŗa£®NaOH””””””b£®H2O2””””””c£®Na2CO3””””d£®CuO | ||
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ijŹµŃ銔×é¶Ō֊ѧæĪ±¾ÖŠæÉÉś³ÉĒāĘųµÄ·“Ó¦½ųŠŠĮĖŃŠ¾æ£¬×ܽį³öČżøöæÉŅŌÉś³ÉH2µÄ·“Ó¦£ŗ¢ŁZn+ŃĪĖį£»¢ŚNa+Ė®£»¢ŪAl+NaOHČÜŅŗ£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ijŹµŃ銔×é¶Ō֊ѧæĪ±¾ÖŠæÉÉś³ÉĒāĘųµÄ·“Ó¦½ųŠŠĮĖŃŠ¾æ£¬×ܽį³öČżøöæÉŅŌÉś³ÉH2µÄ·“Ó¦£ŗ¢ŁZn+ŃĪĖį£»¢ŚNa+Ė®£»¢ŪAl+NaOHČÜŅŗ£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Cu”śCuSO4 | B£® | C”śCO2 | C£® | CuO”śCuSO4 | D£® | Fe2O3”śFe2£ØSO4£©3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com