
烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,并用于烟气脱硫研究。
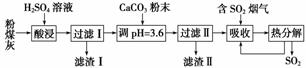
(1)酸浸时反应的化学方程式为________________________________;滤渣Ⅰ的主要成分为________________(填化学式)。
(2)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Al2(SO4)x(OH)6-2x。滤渣Ⅱ的主要成分为________________________(填化学式);若溶液的pH偏高,将会导致溶液中铝元素的含量降低,其原因是
________________________________________(用离子方程式表示)。
(3)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是
________________________________;与吸收SO2前的溶液相比,热分解后循环利用的溶液的pH将________(填“增大”“减小”或“不变”)。
答案 (1)Al2O3+3H2SO4===Al2(SO4)3+3H2O SiO2
(2)CaSO4 3CaCO3+2Al3++3SO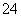 +3H2O===2Al(OH)3+3CaSO4+3CO2↑
+3H2O===2Al(OH)3+3CaSO4+3CO2↑
(3)溶液中的部分SO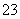 被氧化成SO
被氧化成SO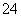 减小
减小
解析 (1)酸浸时能与H2SO4反应的是Al2O3,H2SO4与Al2O3反应生成盐和水,SiO2不和H2SO4反应,成为滤渣。
(2)CaCO3和溶液中的H2SO4反应生成CaSO4;如果pH偏高,一部分Al3+会转化为Al(OH)3沉淀,离子方程式为3CaCO3+2Al3++3SO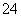 +3H2O===2Al(OH)3+3CaSO4+3CO2↑。
+3H2O===2Al(OH)3+3CaSO4+3CO2↑。
(3)热分解时,一部分亚硫酸盐被氧化为硫酸盐,不能分解成为SO2;SO2溶于水生成H2SO3,会中和溶液中的部分OH-,使溶液的pH减小。


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A.书写热化学方程式时,只要在化学方程式的右端写上热量的符号和数值即可
B.凡是在加热或点燃条件下进行的反应都是吸热反应
C.表明反应所放出或吸收热量的化学方程式叫做热化学方程式
D.氢气在氧气中燃烧的热化学方程式是
2H2(g)+O2(g)===2H2O(l) ΔH=-483.6 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
有关①100 mL 0.1 mol/L NaHCO3、②100 mL 0.1 mol/L Na2CO3两种溶液的叙述不正确的是( )
A.溶液中水电离出的OH—个数:②>① B.溶液中阴离子的物质的量浓度之和:②>①
C.①溶液中:c(CO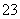 )>c(H2CO3) D.②溶液中:c(HCO
)>c(H2CO3) D.②溶液中:c(HCO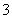 )>c(H2CO3)
)>c(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
用一价离子组成的四种盐溶液:AC、BD、AD、BC,其物质的量浓度均为1 mol/L。在室温下前两种溶液的pH=7,第三种溶液的pH>7,最后一种溶液pH<7,则正确的是( )
| A | B | C | D | |
| 碱性 | AOH>BOH | AOH<BOH | AOH>BOH | AOH<BOH |
| 酸性 | HC>HD | HC>HD | HC<HD | HC<HD |
查看答案和解析>>
科目:高中化学 来源: 题型:
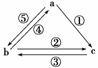
如图所示各步转化关系中,①②③反应是化合反应,④⑤反应是置换反应,则表中各物质之间不能通过一步反应实现如图所示转化关系的是( )
|
| a | b | c |
| A | C | CO2 | CO |
| B | Br2 | FeBr2 | FeBr3 |
| C | Al | AlCl3 | Al2O3 |
| D | Fe | FeCl2 | FeCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:
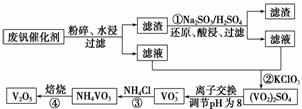
部分含钒物质在水中的溶解性如下:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
回答下列问题:
(1)工业由V2O5冶炼金属钒常用铝热剂法,写出该反应的化学方程式________________。
(2)图中所示滤液中含钒的主要成分为____________(写化学式)。
(3)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,完成反应的离子方程式为 VO
VO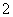 +
+ H2C2O4+
H2C2O4+ ________===
________=== VO2++
VO2++ CO2↑+
CO2↑+ H2O。
H2O。
(4)全钒液流电池的结构如图所示,其电解液中含有钒的不同价态的离子、H+和SO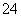 。电池放电时,负极的电极反应为V2+-e-===V3+。
。电池放电时,负极的电极反应为V2+-e-===V3+。
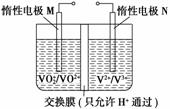
①电池放电时的总反应方程式为__________________。充电时,电极M应接电源的________极;
②若电池初始时左、右两槽内均以VOSO4和H2SO4的混合液为电解液,使用前需先充电激活,充电过程阴极区的反应分两步完成:第一步VO2+转化为V3+;第二步V3+转化为V2+。则第一步反应过程中阴极区溶液n(H+)________(填“增大”、“不变”或“减小”),阳极的电极反应式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
重铬酸钾是一种重要的氧化剂,工业上常用铬铁矿(主要成分为FeO·Cr2O3、SiO2、Al2O3)为原料生产。实验室模拟工业法用铬铁矿制重铬酸钾(K2Cr2O7)的主要工艺如下:
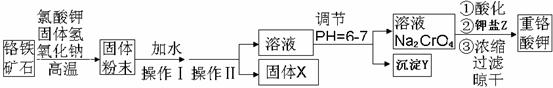
试回答下列问题:
(1)以上工艺流程所涉及元素中属于过渡元素的有 。铁在周期表的位置是 。
(2)操作Ⅱ的名称是 。
(3)固体X的主要成分是___________,沉淀Y的主要成分是 。
(4)流程中①酸化所用的酸和②钾盐Z最合适的是(填符号)________,
A.盐酸和氯化钾 B.硫酸和氯化钾 C.硫酸和硫酸钾 D.次氯酸和次氯酸钾
酸化反应的离子方程式为 。
(5)FeO·Cr2O3与氯酸钾、氢氧化钠高温反应化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3是一种重要的化工原料,可以制备一系列物质(如图)。下列说法正确的是 ( )
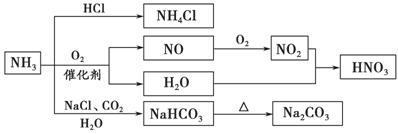
A.NH4Cl和NaHCO3都是常用的化肥
B.NH4Cl、HNO3和Na2CO3受热时都易分解
C.图中所涉及的盐类物质均可发生水解
D.NH3和NO2在一定条件下可以发生氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com