
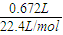 =0.03mol,
=0.03mol,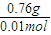 =76g/mol,
=76g/mol,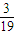 =12g,Y的质量为:76g-12g=64g,
=12g,Y的质量为:76g-12g=64g, =32,
=32,

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2011-2012年浙江省杭州市西湖高级中学高一10月考化学试卷 题型:填空题
(1)下列是关于药物华素片(西地碘片)使用说明书中的部分内容:
华素片(西地碘片)使用说明书
品名:华素片(西地碘片)
英文名:Cydiodine Tablets
成分:本品主要活性成分是分子碘,每片含量1.5mg。利用分
子分散技术将碘制成分子态西地碘,并含适量薄荷脑等。
[贮藏]:遮光、密闭、在阴凉处保存。
[有效期]:三年
(1)①华素片中含有的活性成分是_______(写分子式)
②请推断华素片______(“是”或“不是”)白色。
(2)某学生为验证华素片中含有上述活性成分,完成如下实验,请填写:
①取一粒药片放入研钵中研碎,再将药粉装入试管中,加入约2 mL蒸馏水;再向该试管中再加入约2mL_______(填选项字母),并用力振荡。
| A.酒精 | B.NaOH溶液 | C.四氯化碳 | D.盐酸 |
 的O2中恰好完全燃烧,反应方程式为:
的O2中恰好完全燃烧,反应方程式为:查看答案和解析>>
科目:高中化学 来源:2012-2013学年辽宁省沈阳市四校协作体高一(上)期中化学试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com