
【题目】燃煤产生的烟气中的氮氧化物NOx(主要为NO、NO2)易形成污染,必须经脱除达标后才能排放。
(1)用化学方程式表示NO形成硝酸型酸雨的反应______
(2)能作脱除剂的物质很多,下列说法正确的是______
a.用H2O作脱除剂,不利于吸收含氮烟气中的NO
b.用Na2SO3作脱除剂,O2会降低Na2SO3的利用率
c.用CO作脱除剂,会使烟气中NO2的浓度增加
(3)尿素[CO(NH2)2]在一定条件下能有效将NOx转化为N2
Ⅰ.已知可通过下列方法合成尿素:2NH3(g)+CO2(g)![]() H2NCOONH4(s)△H=-159.5kJ/mol
H2NCOONH4(s)△H=-159.5kJ/mol
H2NCOONH4(s)![]() CO(NH2)2(s)+H2O(l) △H=+28.5kJ/mol
CO(NH2)2(s)+H2O(l) △H=+28.5kJ/mol
①尿素释放出NH3的热化学方程式是______。
②写出有利于尿素释放NH3的条件并说明理由______。
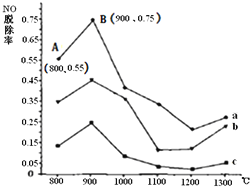
ⅡCO(NH2)2与某种烟气![]() 主要为N2、NO和O2)中的NO的物质的量比值分别为1:2、2:1、3:1时,NO脱除率随温度变化的曲线如图:
主要为N2、NO和O2)中的NO的物质的量比值分别为1:2、2:1、3:1时,NO脱除率随温度变化的曲线如图:
①曲线a对应CO(NH2)2与NO的物质的量比值是______。
②曲线a、b、c中,800℃~900℃区间内发生主要反应的化学方程式是______。
③900℃~1200℃区间内脱除率下降,NO浓度上升,发生的主要反应是______。
④曲线a中,NO的起始浓度为6×10-4mg/m3,从A点到B点经过0.8s,该时间段内NO的脱除速率为______mg/(m3·s) 。
【答案】2NO+O2=2NO2,3NO2+H2O=2HNO3+NO ab CO(NH2)2(s)+H2O(l)![]() 2NH3(g)+CO2(g) △H=+131kJ/mol 升高温度有利于平衡向吸热的正反应方向进行,同时温度升高,氨气的溶解度降低,均有利于向释放氨气的方向进行
2NH3(g)+CO2(g) △H=+131kJ/mol 升高温度有利于平衡向吸热的正反应方向进行,同时温度升高,氨气的溶解度降低,均有利于向释放氨气的方向进行 ![]() :1 4NH3+6NO
:1 4NH3+6NO![]() 5N2+6H2O或2CO(NH2)2+6NO
5N2+6H2O或2CO(NH2)2+6NO![]() 2CO2+4H2O+5N2 4NH3+5O2
2CO2+4H2O+5N2 4NH3+5O2![]() 4NO+6H2O 1.5×10-4
4NO+6H2O 1.5×10-4
【解析】
(1)NO被O2氧化产生NO2,NO2与水反应产生HNO3和NO;
(2)a.一氧化氮不易溶于水,而二氧化氮易溶于水,反应生成NO;
b.亚硫酸钠不稳定,易被氧气氧化;
c.用CO作脱除剂,则氮氧化物得电子发生还原反应;
(3)Ⅰ.①根据盖斯定律,将两个热化学方程式相加,然后进行颠倒即得目标方程式,其焓变进行相应改变;
②尿素释放NH3的反应是吸热反应,根据温度对化学平衡及氨气溶解度的影响进行分析;
Ⅱ.①CO(NH2)2的含量越高,NO脱除率越高;
②800℃~900℃区间内NO脱除率增大,NO参加反应,即尿素与NO反应生成N2;
③900℃~1200℃区间内脱除率下降,NO浓度上升,反应中应该生成NO;
④A点到B点,NO脱除率由0.55变为0.75,故NO的浓度变化量为(0.75-0.55)×6×10-4 mg/m3=1.2×10-4 mg/m3,再利用![]() 计算NO的脱除速率。
计算NO的脱除速率。
(1)一氧化氮不稳定,易和氧气反应生成二氧化氮,二氧化氮和水反应生成硝酸和一氧化氮,故NO形成硝酸型酸雨的反应为2NO+O2=2NO2,3NO2+H2O=2HNO3+NO;
(2)a.一氧化氮不溶于水,而二氧化氮易溶于水,反应生成NO,不利于吸收含氮烟气中的NO,a正确;
b亚硫酸钠不稳定,易被氧气氧化,O2会降低Na2SO3的利用率,b正确;
c.用CO作脱除剂,被氧化,则氮氧化物得电子发生还原反应,不生成NO2,烟气中NO2的浓度不增加,c错误;
故答案选ab;
(3)①已知:2NH3(g)+CO2(g)![]() H2NCOONH4(s) △H=-159.5kJ/mol
H2NCOONH4(s) △H=-159.5kJ/mol
H2NCOONH4(s)![]() CO(NH2)2(s)+H2O(l) △H=+28.5kJ/mol
CO(NH2)2(s)+H2O(l) △H=+28.5kJ/mol
根据盖斯定律,将两个热化学方程式相加,整理可得2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(l) △H=-131kJ/mol ,所以尿素释放出NH3的热化学方程式为:CO(NH2)2(s)+H2O(l)
CO(NH2)2(s)+H2O(l) △H=-131kJ/mol ,所以尿素释放出NH3的热化学方程式为:CO(NH2)2(s)+H2O(l)![]() 2NH3(g)+CO2(g) △H=+131kJ/mol;
2NH3(g)+CO2(g) △H=+131kJ/mol;
②根据①分析可知:释放氨气的反应是吸热反应,升高温度,有利于化学平衡向吸热的正反应方向进行,同时温度升高,氨气的溶解度降低,均有利于向释放氨气的方向进行;
Ⅱ.①CO(NH2)2的含量越高,NO的转化率越大,即NO脱除率越高,所以曲线a 对应CO(NH2)2 与NO的物质的量比值是3:1;
②800℃~900℃区间内NO脱除率增大,所以NO是作为反应物参加反应,高温时,尿素分解生成氨气、二氧化碳,氨气和一氧化氮发生氧化还原反应生成氮气,即尿素与NO反应生成N2,同时生成二氧化碳和水,所以反应方程式为:4NH3+6NO![]() 5N2+6H2O或 2CO(NH2)2+6NO
5N2+6H2O或 2CO(NH2)2+6NO![]() 2CO2+4H2O+5N2;
2CO2+4H2O+5N2;
③900℃~1200℃区间内脱除率下降,所以NO浓度上升,则该反应中应该有NO生成,尿素分解生成的氨气和烟气中的氧气反应生成一氧化氮和水,导致NO浓度增大,所以反应方程式为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
④A点到B点NO脱除率由0.55变为0.75,则NO的浓度变化量为(0.75-0.55)×6×10-4 mg/m3=1.2×10-4mg/m3,所以NO的脱除速率=![]() =1.5×10-4mg/(m3·s)。
=1.5×10-4mg/(m3·s)。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】有机物A、B均为合成某种抗支气管哮喘药物的中间体,A在一定条件下可转化为B(如下图所示),下列说法正确的是
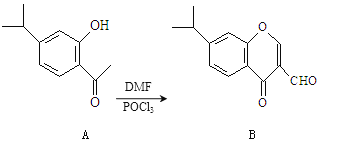
A.分子A中所有碳原子均位于同一平面
B.用FeCl3溶液可检验物质B中是否混有A
C.物质B既能发生银镜反应,又能发生水解反应
D.1mol B最多可与5mol H2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示。
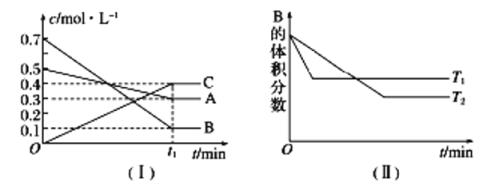
根据以上条件,回答下列问题:
(1)A与B反应生成C的化学方程式为________,正反应为_____(填“吸热”或“放热”)反应。
(2)t1 min后,改变下列某一条件,能使平衡向逆反应方向移动的有______(填字母序号)。
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.保持其他条件不变,升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g)![]() Z(g)+W(s) ΔH>0。下列叙述正确的是( )
Z(g)+W(s) ΔH>0。下列叙述正确的是( )
A. 加入少量W,逆反应速率增大,正反应速率减小 B. 升高温度,平衡逆向移动
C. 当容器中气体压强不变时,反应达到平衡 D. 反应平衡后加入X,上述反应的ΔH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙(CaO2)微溶于水,溶于酸,可作分析试剂、医用防腐剂、消毒剂。以下是一种制备过氧化钙的实验方法。回答下列问题:
I.过氧化钙的制备。流程如下,步骤②的装置示意图为图一:
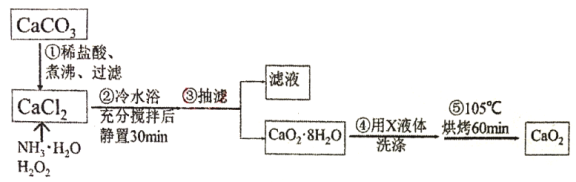

(1)步骤①将溶液煮沸、过滤。将溶液煮沸的目的是___。
(2)图一装置中:①仪器a的名称是___;
②反应的化学方程式为___;
③该反应需要在冷水浴中进行,原因是___。
(3)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是___。
Ⅱ.过氧化钙的测定:已知CaO2在350℃时迅速分解生成CaO和O2。该小组采用如图二所示装置测定刚才制备的产品中CaO2的纯度(设杂质不分解产生气体)
(1)量气管读数时需注意的项有:①气体冷却到室温;②量气装置两侧液面相平;③___。
(2)使用电子天平准确称取0.5000g样品,置于试管中加热使其完全分解,收集到33.60mL(已换算为标准状况)气体,则产品中CaO2的质量分数为___(保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“煤制油”的关键技术是煤的气化,目前煤的气化主要是煤中的碳和水蒸气反应: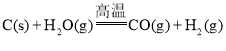 ,该反应是吸热反应,反应所需能量是由间歇进行的碳的燃烧(氧气用空气代替)来提供的:
,该反应是吸热反应,反应所需能量是由间歇进行的碳的燃烧(氧气用空气代替)来提供的: 。下列说法不正确的是( )
。下列说法不正确的是( )
A.煤的气化可以减少煤直接燃烧对环境造成的粉尘污染
B.第一个反应需要吸热,所以煤的气化从能量角度来看,得不偿失
C.煤气化后作为燃料,燃烧充分,热利用率高
D.上述两个反应,反应后的混合气体中除去![]() 、
、![]() 后主要是合成氨的两种原料气体
后主要是合成氨的两种原料气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实能用勒夏特列原理解释的是( )
A.工业上N2与H2合成NH3,往往需要使用催化剂
B.密闭容器中2molCO与1molH2O(g)充分反应达平衡后,增大压强CO的反应速率加快
C.SO2与O2催化氧化成SO3是一个放热过程,450℃左右的温度比室温更有利于SO3生成
D.向1.50mol/L的硝酸铵溶液中加入少量氨水至中性,水的电离程度减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项内容,排列顺序正确是( )
①固体的热稳定性:Na2CO3>CaCO3>NaHCO3
②常见离子的还原性排序:S2->I->Fe2+
③微粒半径:K+>S2->F-
④给出质子的能力:CH3COOH>C2H3OH>H2O
⑤氢化物的沸点:H2Se>H2S>H2O
A.①③B.②④C.①②D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五倍子是一种常见的中草药,其有效成分为X。一定条件下X可分别转化为Y、Z,如下所示。
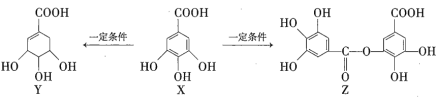
下列说法错误的是( )
A.![]() 最多能与
最多能与![]() 发生取代反应
发生取代反应
B.等物质的量的Z分别与Na和![]() 恰好反应时,消耗Na和
恰好反应时,消耗Na和![]() 的物质的量之比为6∶1
的物质的量之比为6∶1
C.一定条件下,Y能发生加成反应、取代反应、消去反应和氧化反应
D.![]() 最多能与
最多能与![]() 发生反应
发生反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com