
 能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务.阅读下列有关能源的材料,回答有关问题:
能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务.阅读下列有关能源的材料,回答有关问题:分析 (1)断开化学键要吸收能量,形成化学键要释放能量,据此回答;
(2)原电池是将化学能转化为电能的装置,其中活泼金属做负极发生氧化反应,正极得电子发生还原反应;根据原电池的工作原理结合电子转移进行计算即可.
解答 解:(1)在化学反应中,化学反应的实质是旧键的断裂和新键的生成,断开化学键要吸收能量,形成化学键要释放能量,故答案为:吸收能量,释放能量;
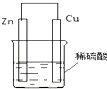
(2)原电池是将化学能转化为电能的装置,其中活泼金属Zn做负极,发生氧化反应Zn-2e-=Zn2+;正极氢离子得电子发生还原反应2H++2e-=H2↑,当导线中有2mol电子通过时,产生氢气是1mol,质量是2g.
故答案为:化学,电;Zn-2e-=Zn2+;氧化;产生气泡;还原;锌片;铜片;2g.
点评 本题考查化学反应的实质、原电池中电极反应式书写及电子守恒的计算知识,题目难度不大.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2OH?CH2=CH2(g)+H2O(g);△H>0 | |
| B. | CO2(g)+H2(g)?CO(g)+H2O(g);△H>0 | |
| C. | CO2(g)+2NH3( g)?CO(NH2)2(s)+H2O(g);△H<0 | |
| D. | 2C6H5CH2CH3(g)+O2(g)?2C6H-5CH=CH2(g)+2H2O(g);△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①③④⑤ | C. | ②④⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
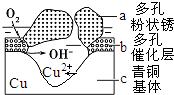 我国古代青铜器工艺精湛,有很高的艺术价值和历史价值.但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义.
我国古代青铜器工艺精湛,有很高的艺术价值和历史价值.但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜和浓硝酸为原料生产硝酸铜 | B. | 甲烷与氯气制备一氯甲烷 | ||
| C. | 乙烯与HCl制取氯乙烷 | D. | 由反应2SO2+02?2SO3制SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)×c(OH-)=1×10-14 | B. | 该溶液中由水电离出的c(H+)=1×10-7 | ||
| C. | c(H+)=c(OH-)=1×10-7 | D. | c(H+)×c(OH-)=1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com