
下列各图中,表示吸热反应的是()
A.  B.
B.  C.
C. 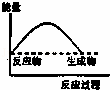 D.
D. 
科目:高中化学 来源: 题型:
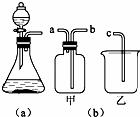
如图是实验室制取气体的一种发生装置.
(1)若用上述装置制取O2,除了可选择二氧化锰和 (物质名称)反应外,还能选择 (填物质的化学式)和水反应,写出后一个反应的化学方程式: .
(2)用排空气法收集H2,可选择图(b)中的甲装置,收集时气体应从 口进气.(填“a”或“b”)
(3)实验室以KMnO4和浓盐酸为反应物,利用(a)、(b)装置组合制取氯气,反应方程式如下:
2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O
①配平上述反应方程式(在空格里填上适合的化学计量数).
②组合装置乙中盛放氢氧化钠溶液,其作用为 ,发生反应的离子方程式为 .
(4)广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其他简单仪器组成各种用途的装置.
如充当集气瓶,还可作 , (填写两种即可).
查看答案和解析>>
科目:高中化学 来源: 题型:
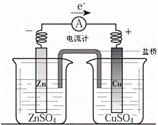
关于图所示装置(盐桥含KCl)的叙述,正确的是( )
|
| A. | 铜离子在铜片表面被氧化 |
|
| B. | 铜作阳极,铜片上有气泡产生 |
|
| C. | 电流从锌片经导线流向铜片 |
|
| D. | 如图烧杯中,SO42﹣的物质的量几乎不变,K+的数目增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1~18号元素的离子aW3+、bX+、cY2﹣、dZ﹣都具有相同的电子层结构,下列关系正确的是()
A. 质子数c>b B. 离子的还原性Y2﹣>Z﹣
C. 氢化物的稳定性H2Y>HZ D. 原子半径X<W
查看答案和解析>>
科目:高中化学 来源: 题型:
下表列出了a﹣f六种元素在周期表前三周期的位置.
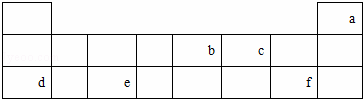
请回答下列问题:
(1)c元素的名称是氧,d元素位于IA族.
(2)用元素符号表示,六种元素中,性质最稳定的元素原子结构示意图 , 元素的原子半径最大.
(3)非金属性b c.(填“大于”“小于”)
(4)用化学式表示,六种元素中,最高价氧化物属于两性氧化物的是 ,最高价氧化物对应水化物酸性最强的是 4
(5)写出d元素单质与水反应的离子方程式
(6)写出e元素单质与NaOH反应的离子方程式
(7)用电子式表示化合物d2c的形成过程 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中,正确的是()
A. 含金属元素的离子一定都是阳离子
B. 在氧化还原反应中,非金属单质一定是氧化剂
C. 某元素从化合态变为游离态时,该元素一定被还原
D. 金属阳离子被还原不一定得到金属单质
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等.下列反应与Br2+SO2+2H2O=H2SO2+2HBr相比较,水的作用相同的是()
A. 电解水:2H20=2H2↑+O2↑ B. 4Fe(OH)2+O2+2H2O=4Fe(OH)3
C. 2F2+H2O=4HF+O2 D. 3NO2+H2O=2HNO3+NO
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A(g)+B(g)⇌C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ 700 800 830 1000 1200
平衡常数 1.7 1.1 1.0 0.6 0.4
830℃时,向一个2L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4s内A的平均反应速率v(A)=0.005mol/(L•s).下列说法正确的是()
A. 4s时c(B)为0.76mol/L
B. 830℃达平衡时,A的转化率为80%
C. 反应达平衡后,升高温度,平衡正向移动
 D. 1200℃时反应C(g)+D(g)⇌A(g)+B(g)的平衡常数的值为0.
D. 1200℃时反应C(g)+D(g)⇌A(g)+B(g)的平衡常数的值为0. 4
4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com