
【题目】浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。下列有关该电池的说法错误的是

A. 电池工作时,Li+通过离子电子导体移向b区
B. 电流由X极通过外电路移向Y极
C. 正极发生的反应为:2H++2e-=H2↑
D. Y极每生成1 mol Cl2,a区得到2 mol LiCl
科目:高中化学 来源: 题型:
【题目】砷(As)及其化合物在生产、医疗、科技等方面有许多应用
(1)中国自古“信口雌黄”、“雄黄入药”之说。雄黄As2S3和雌黄As4S4都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。一定条件下,雌黄和雄黄的转化关系如图所示。

①砷元素有+2、+3+5等常见价态。,雌黄和雄黄中S元素的价态相同,其价态是______________。I中发生的离子方程式是______________________________。
②Ⅱ中,雄黄在空气中加热至300℃时会产生两种物质,若4.28g As4S4反应转移0.28mole-,则a为_______________(填化学式)砒霜(As2O3)可用双氧水将氧化成H3AsO4而除去,该反应的化学方程式为:____________________________________。
(2)AsH3是一种很强的还原剂,室温下, 0.4mol AsH3气体在空气中自燃,氧化产物为As2O3固体,放出b kJ 热量,AsH3自燃的热化学方程式是:____________________________________。
(3)将Na3AsO3(aq)+I2(aq)+H2O(l)![]() Na2HasO4(aq)+NaI (aq)设计成原电池如图所示,放电时电流强度(I)与时间关系如图所示.
Na2HasO4(aq)+NaI (aq)设计成原电池如图所示,放电时电流强度(I)与时间关系如图所示.
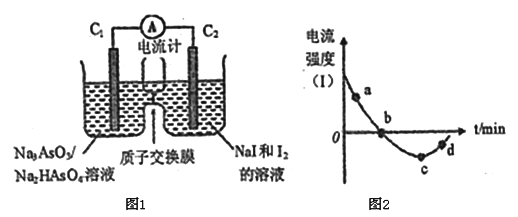
①如图中表示在该时刻上述可逆反应达到平衡状态的点是_________________(填字母)。
②已知:a点对应如图中电流由C1极经外电路流向C2极。则d点对应的负极的反应式为_____________。
③如图中,b→c改变条件可能是____________(填代号),c→d电流强度变化的原因是___________。
A.向左室中加入适量的浓Na3AsO3溶液 B.向左室中加入适量的烧碱溶液
C.向右室中加入适量的浓KI溶液 D. 向右室中加入适量的稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
①CH4(g)+2O2(g)![]() CO2(g)+2H2O(l) ΔH=890 kJ·mol1
CO2(g)+2H2O(l) ΔH=890 kJ·mol1
②2C2H6(g)+7O2(g)![]() 4CO2(g)+6H2O(l) ΔH=3116.7 kJ·mol1
4CO2(g)+6H2O(l) ΔH=3116.7 kJ·mol1
③C2H4(g)+3O2(g)![]() 2CO2(g)+2H2O(l) ΔH=1409.6 kJ·mol1
2CO2(g)+2H2O(l) ΔH=1409.6 kJ·mol1
④2C2H2(g)+5O2(g)![]() 4CO2(g)+2H2O(l) ΔH=2596.7 kJ·mol1
4CO2(g)+2H2O(l) ΔH=2596.7 kJ·mol1
⑤C3H8(g)+5O2(g)![]() 3CO2(g)+4H2O(l) ΔH=2217.8 kJ·mol1
3CO2(g)+4H2O(l) ΔH=2217.8 kJ·mol1
现由上述五种烃中的两种组成的混合气体2 mol,经充分燃烧后放出3037.6 kJ热量,则下列哪些组合是不可能的
A.C2H4和C2H6 B.C2H2和C3H8 C.C2H6和C3H8 D.C2H6和CH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组在实验室中利用下图装置(夹持装置略去)测定某铁硫化物(FexSy)的组成,并探究反应后D装置所得溶液中含硫化合物的组成。

(一)硫化物(FexSy)的组成
实验步骤:
步骤Ⅰ 如图连接装置,检査装置气密性,装入药品;
步骤Ⅱ 打开分液漏斗旋塞,缓缓滴入水,并点燃酒精喷灯;
步骤Ⅲ 当硬质玻璃管中固体质量不再改变时,停止加热,继续通入—段时间的O2
步骤Ⅳ 实验结束后,将D中所得溶液加水配制成250 mL溶液;
……
请回答:
⑴仪器a的作用为______________________。
(2)步骤Ⅲ中,停止加热后还需继续通入一段时间的O2,其目的为__________________。
(3)步骤IV中配制溶液时所需的玻璃仪器除玻璃棒和烧杯外,还有___________________。
(4)取25. 00 mL步骤IV中所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为4.66g。则FexSy的化学式为___________________。
(5)问题讨论:有同学认为可将装置D改为装有足量碱石灰的干燥管,通过测定反应前后干燥管的增重来计算硫元素的含量。你认为此方案________(填“是”或“否”)合理,原因为_______________________。
(二)探究反应后D装置所得溶液中含硫化合物的组成。
理论推测:溶液中除含有Na2SO4外,还可能含有Na2SO3。
实验探究:滴定法测定溶液中Na2SO3的含量。
可供选择的试剂:①0.10 mol L-1 KmnO4酸性溶液 ②30%H2O2
③0.10 mol L-1 KI淀粉溶液
(6)所选试剂为___________(填序号);所选试剂应装在_____________(填“酸式”或“碱式”)滴定管中。
⑦所利用的反应原理为__________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学平衡常数的叙述,正确的是( )
A.化学平衡常数只与反应的温度有关
B.化学平衡常数只与化学反应方程式本身和温度有关
C.化学平衡常数与化学反应本身和温度有关,并且会受到起始浓度的影响
D.化学平衡常数只与化学反应本身有关,与其他任何条件无关的一个不变的常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7是一种橙红色固体,可用于火柴制造、电镀、有机合成等方面。用某酸性废液(主要含Cr3+、还含有少量Fe2+、Fe3+和Al3+等)制备的流程如下:
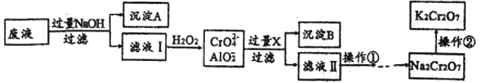
已知:H++CrO2-+H2O![]() Cr(OH)3
Cr(OH)3![]() Cr3++3OH-
Cr3++3OH-
回答下列问题:
(1)沉淀A的主要成分是_____________(填化学式,下同),流程中的X是__________。
(2)滤液Ⅰ中铬元素的存在形式主要是_____________(填离子符号)。
(3)操作是向滤液中加入稀硫酸调PH至一定范围。在酸性环境中CrO42-转化为Cr2O72-,溶液变为橙红色,该转化的离子方程式是__________;若PH高于此范围,造成的影响是__________。
(4)操作②是向Na2Cr2O7溶液中加入KCl固体后得到K2Cr2O7,说明相同温度下,在水中的溶解度:Na2Cr2O7______________ K2Cr2O7(填“>”、“<”或“=”)。
(5)PbO2可直接将溶液中的Cr3+氧化成Cr2O72-,该反应的离子方程式是__________。
(6)K2Cr2O7可用来测定溶液中Fe2+的含量,还原产物为Cr3+。若1L FeSO4溶液与100mL 0.1mol/L K2Cr2O7溶液恰好完全反应,则c(FeSO4)=___________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修5:有机化学基础】
化合物F是一种重要的有机合成中间体。下面是以化合物A为原料合成化合物F的路线:

回答下列问题:
(1)化合物E中含氧官能团的名称是________________。
(2)以羟基为取代基,化合物A的化学名称是________________,A分子中最多有_______个原子共平面。
(3)D生成E的反应类型为_________________,由C生成D的化学方程式为_____________________。
(4)满足下列条件的E的芳香族同分异构体共有____________种(不含立体异构);
①能发生银镜反应和水解反应
②其水解产物之一能与FeCl3溶液发生显色反应
其中核磁共振氢谱显示为四组峰,且峰面积比为1∶2∶3∶6的一种同分异构体的结构简式为________________________。
(5)参照上述合成路线,以![]() 和CH2(COOH)2为原料(其他试剂任选),设计制备
和CH2(COOH)2为原料(其他试剂任选),设计制备![]() 的合成路线[已知:
的合成路线[已知:![]() ]:_________________________________________________________。
]:_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两个容积均为10L的密闭容器Ⅰ和Ⅱ中发生反应:2NO(g)+2CO(g) ![]() N2(g)+2CO2(g),起始物质的量见下表。实验测得两容器不同温度下达到平衡时CO2的物质的量浓度如下图所示,下列说法错误的是
N2(g)+2CO2(g),起始物质的量见下表。实验测得两容器不同温度下达到平衡时CO2的物质的量浓度如下图所示,下列说法错误的是

容器 | 起始物质的量 | ||
NO | CO | ||
Ⅰ | 1mol | 0.5mol | |
Ⅱ | 2mol | 1mol | |
A. 反应N2(g)+2CO2(g)![]() 2NO(g)+2CO(g)的ΔH<0,ΔS>0
2NO(g)+2CO(g)的ΔH<0,ΔS>0
B. P点的速率比M点慢
C. M、N两点容器内的压强: P(M) <2P(N)
D. N点的平衡常数为44.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素Se位于第四周期ⅥA族,下列说法不正确的是
A. Se的原子序数为34
B. 单质Se在空气中燃烧可生成SeO3
C. 可形成Na2SeO3、Na2SeO4两种盐
D. H2S比H2Se稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com