
| A. | $\frac{a+b}{5}×100%$ | B. | $\frac{2(a+b)}{5b}×100%$ | C. | $\frac{2(a+b)}{5}×100%$ | D. | $\frac{a+b}{5a}×100%$ |
分析 设y转化的物质的量为mmol,
x+2y═2z
amol bmol 0
0.5mmol mmol mmol
(a-0.5m)mol (b-m)mol mmol
因为 n(x)+n(y)=n(z),所以(a-0.5m)mol+(b-m)mol=mmol,据此计算m值,再根据转化率公式计算转化率.
解答 解:设y转化的物质的量为mmol,
x+2y═2z
amol bmol 0
0.5mmol mmol mmol
(a-0.5m)mol (b-m)mol mmol
因为 n(x)+n(y)=n(z),所以(a-0.5m)mol+(b-m)mol=mmol,
a-0.5m+b-m=m,
m=$\frac{a+b}{2.5}$,y的转化率=$\frac{\frac{a+b}{2.5}mol}{bmol}×100%$=$\frac{2(a+b)}{5b}×100%$,故选B.
点评 本题考查化学平衡有关计算,明确各个物理量的关系是解本题关键,利用“三段式”法分析解答即可,题目难度不大.


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:解答题
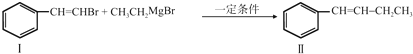
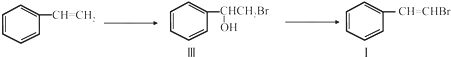
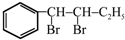 .
. ;(注明反应条件)
;(注明反应条件)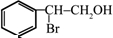 ,Ⅴ的结构简式为
,Ⅴ的结构简式为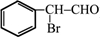 .
.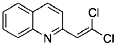 与BrMgCH2(CH2)3CH2MgBr在一定条件下发生类似反应①的反应,生成的有机化合物Ⅵ(分子式为C16H17N)的结构简式为
与BrMgCH2(CH2)3CH2MgBr在一定条件下发生类似反应①的反应,生成的有机化合物Ⅵ(分子式为C16H17N)的结构简式为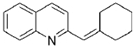 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 充电时阴极发生氧化反应 | |
| B. | 放电时负极的电极反应为CH3OH+8OH--6e-═CO32-+6H2O | |
| C. | 通入0.25mol氧气并完全反应后,有1mol电子转移 | |
| D. | 放电时阴离子向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇的水溶液可使蛋白质发生性质改变 | |
| B. | 纤维素在一定条件下水解生成葡萄糖 | |
| C. | 在一定条件下油脂水解可生成甘油 | |
| D. | 煤的干馏、石油的分馏都属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
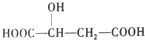 ,下列说法错误的是( )
,下列说法错误的是( )| A. | 1mol苹果酸可与2 molNaOH发生中和反应 | |
| B. | -定条件下,苹果酸与乙酸或乙醇均能发生酯化反应 | |
| C. |  与苹果酸互为同分异构体 与苹果酸互为同分异构体 | |
| D. | 1mol苹果酸与足量金属Na反应生成1.5 molH 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生活中用食盐水制取消毒液应用的是电解原理 | |
| B. | 自然界中无游离态的钠、钾、硅,有游离态的铁、硫、氧 | |
| C. | 合金属于金属材料,陶瓷属于非金属材料,化纤属于有机高分子材料 | |
| D. | 泡沫灭火器中用硫酸铝与饱和小苏打溶液反应,与盐类的水解知识无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向氯化铁溶液中滴加HI溶液:2Fe3++2HI═2Fe2++2H++I2 | |
| B. | 向NH4Al(SO4)2溶液中滴入Ba(0H)2恰好使反应完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4+AlO2-+2H2O | |
| C. | 1mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积均匀混合2AlO2-+5H+═Al(OH)3+Al3++H2O | |
| D. | 用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2═I2+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C5H12的烃有三种可能的结构 | |
| B. | 乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色 | |
| C. | 苯乙烯在合适条件下催化加氢可生成乙基环己烷 | |
| D. | 淀粉、纤维素和蛋白质都是高分子化合物,它们在一定条件下都能水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
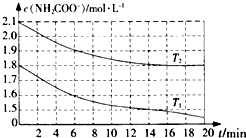 科学研究小组对氨基甲酸铵(NH2COONH4)的分解和水解反应进行探究.
科学研究小组对氨基甲酸铵(NH2COONH4)的分解和水解反应进行探究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com