
| A. | 阴阳离子间通过静电吸引形成的化学键叫做离子键 | |
| B. | HF,HCl,HBr,HI的热稳定性和酸性均依次减弱 | |
| C. | 元素非金属越强,其对应含氧酸的酸性就越强 | |
| D. | 元素周期律是元素原子核电子排布周期性变化的结果 |
分析 A.阴阳离子间通过静电作用形成的化学键叫做离子键;
B.根据HF,HCl,HBr,HI中H-X键强弱判断,H-X越弱热稳定性减弱,酸性增强;
C.元素非金属越强,其对应最高价含氧酸的酸性就越强;
D.原子结构中核外电子排布的周期性变化而引起元素的性质呈周期性变化.
解答 解:A.阴阳离子间通过静电作用形成的化学键叫做离子键,静电作用包含吸引、排斥等作用,故A错误;
B.同主族自上而下非金属性减弱,HF,HCl,HBr,HI中H-X键减弱,故HF,HCl,HBr,HI的热稳定性减弱,酸性增强,故B错误;
C.元素非金属越强,其对应最高价含氧酸的酸性就越强,不是最高价含氧酸,酸性不一定强,如HClO属于弱酸,酸性比碳酸弱,故C错误;
D.因原子结构中核外电子排布的周期性变化而引起元素的性质呈周期性变化,元素的性质呈周期性变化的根本原因是核外电子排布的周期性变化的结果,故D正确;
故选D.
点评 本题考查了化学键与物质性质关系、元素周期律等,题目难度不大,注意规律的理解掌握与特殊性.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2O C2H4O2 | B. | C2H4 C2H4O | C. | 乙烯 聚乙烯 | D. | C8H8 C4H8O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 14Si | 15P | 16S | 17Cl | |
| 单质与H2 反应的条件 | 高温 | 磷蒸气与 H2能反应 | 加热 | 光照或点燃 时发生爆炸 |
| 最高价氧化 物的水化物 | H4SiO4 弱酸 | H3PO4中强酸 | H2SO4 强酸 | HClO4 最强含氧酸 |
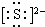 K+ PCl3
K+ PCl3 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com