
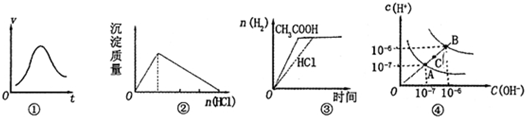
| A、图①表示一定条件下某化学反应的速率随时间变化的趋势图,该反应一定为放热反应 | B、图②表示在四羟基合铝酸钠溶液中加入盐酸,产生沉淀的质量变化 | C、图③表示等体积、等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁粉,产生H2的物质的量的变化 | D、图④为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2013-2014学年湖北省高三上学期12月月考化学试卷(解析版) 题型:选择题
下列各示意图与对应的表述正确的是 ( )
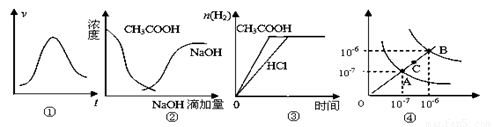
A.图①表示一定条件下某化学反应的速率随时间变化的趋势图,该反应一定为放热反应
B.图②中曲线表示将氢氧化钠溶液滴加到醋酸溶液浓度的变化趋势图
C.图③表示等体积、等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁粉,产生H2的物质的量的变化
D.图④为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法
查看答案和解析>>
科目:高中化学 来源:2014届东北三省四市教研协作体高三联合考试理综化学试卷(解析版) 题型:选择题
下列各示意图与对应的表述正确的是
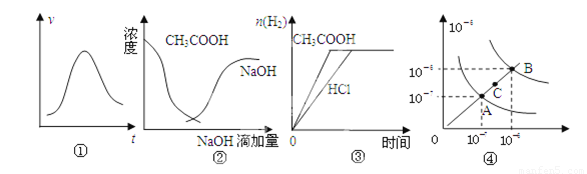
A.图①表示一定条件下某化学反应的速率随时间变化的趋势图,该反应一定为放热反应
B.图②中曲线表示将氢氧化钠溶液滴加到醋酸溶液浓度的变化趋势图
C.图③表示等体积、等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁粉,产生H2的物质的量的变化
D.图④为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各示意图与对应的表述正确的是 ( )
A.图①表示一定条件下某化学反应的速率随时间变化的趋势图,该反应一定为放热反应
B.图②中曲线表示将氢氧化钠溶液滴加到醋酸溶液浓度的变化趋势图
C.图③表示等体积、等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁粉,产生H2的物质的量的变化
D.图④为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法

查看答案和解析>>
科目:高中化学 来源: 题型:
下列各示意图与对应的表述正确的是
A.图①表示一定条件下某化学反应的速率随时间变化的趋势图,该反应一定为放热反应
B.图②中曲线表示将氢氧化钠溶液滴加到醋酸溶液浓度的变化趋势图
C.图③表示等体积、等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁粉,产生H2的物质的量的变化
D.图④ 为水的电离平衡曲线图,若从A点到C点,可采用在水中加入适量NaOH固体的方法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com