
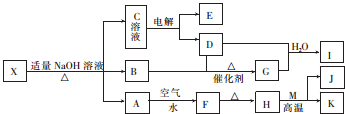
分析 F是一种红褐色沉淀,则F为Fe(OH)3,可推知A为Fe(OH)2,则H为,M、K是常见的金属单质,结合H与M反应的条件可知,H为Fe2O3,M为Al,K为Fe,J为Al2O3,X与氢氧化钠反应生成的B是一种有刺激性气味的气体,则要推知B为NH3,向C溶液中加入 BaCl2溶液,生成不溶于稀盐酸的白色沉淀,则C中有Na2SO4,电解后可产生氧气和氢气,氧气能氧化氨气,所以D为O2,E为H2,氨气被氧气氧化成G为NO,所I为HNO3,结构A、B、C的成分可知X中有亚铁离子、铵根离子、硫酸根离子,X不带结晶水,则X为(NH4)2Fe(SO4)2,以此解答该题.
解答 解:(1)根据上面的分析可知,X的化学式为(NH4)2Fe(SO4)2,
故答案为:(NH4)2Fe(SO4)2;
(2)根据反应4NO+3O2+2H2O=4HNO3可知,反应时NO和O2的物质的之比为4:3,
故答案为:4:3;
(3)足量的铁与硝酸的稀溶液反应的离子方程式为3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,
故答案为:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O;
(4)I与NaOH溶液恰好完全反应可生成一种盐为NaNO3,将该盐的水溶液蒸干灼烧可得到NaNO2,
故答案为:NaNO2;
(5)X为(NH4)2Fe(SO4)2,在0.02mol•L-1的X溶液中,由于亚铁离子和铵根离子都能水解,所以各种离子的浓度由大到小的顺序为 c(SO42-)>((NH4+)>c(Fe2+)>((H+)>(OH-),
故答案为:c(SO42-)>((NH4+)>c(Fe2+)>((H+)>(OH-).
点评 本题考查了无机物的推断,为高考常见题型和高频考点,涉及Fe与N元素化合物转化、电解、常用化学用语、铝热反应等,正确推断物质是解本题关键,F是一种红褐色沉淀为突破口,采用正逆相结合的方法推断,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 2,3,3一三甲基戊烷 | B. | 2-甲基-2-丁烯 | ||
| C. | 3,3一二甲基-4-乙基戊烷 | D. | 3,3,4一三甲基已烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
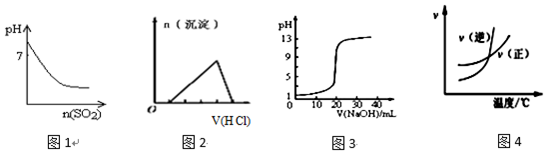
| A. | 图1表示将SO2气体通入溴水中,所得溶液的pH变化 | |
| B. | 图2表示向含有少量氢氧化钠的偏铝酸钠溶液中滴加盐酸所得沉淀的物质的量与盐酸体积的关系 | |
| C. | 图3表示常温下,向0.1000mol•L-1HCl溶液中滴加20.00mL 0.1000mol•L-1氨水的滴定曲线 | |
| D. | 图4表示乙醇的催化氧化反应中速率随温度的变化图象,升高温度该反应的平衡常数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④⑥ | C. | ①④⑤ | D. | ①③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com